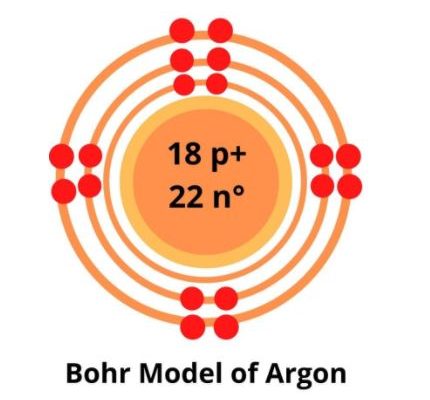
氩是原子序数为18的第18族元素。它用符号Ar表示,是惰性气体。它也是地球大气中含量第三多的气体。空气中氩的质量比约为1.288%,可通过分馏分离出来。
它是工业用氩的主要来源。氩气主要用于需要惰性气氛的工业,如钛的制备。
本文将逐步讨论氩的玻尔图。
氩的玻尔模型
1911年提出的卢瑟福原子模型无法解释电子在原子核周围运动时的稳定性。
根据经典力学和电磁理论,这种粒子不能保持稳定,会失去能量。
尼尔·玻尔修正了这个模型,并在1913年提出了临时的玻尔-卢瑟福原子模型。在这个模型中,他假设每个电子都在一个预先确定的轨道上运动,具有固定的大小和能量。
玻尔原子模型定义元素的原子结构,通过一个图像表示所有的原子粒子,即电子、质子和中子。
在我们深入研究原子的玻尔模型之前,我们首先应该理解几个用于描述原子结构的与这个模型有关的重要术语。
•核:原子的中心或核心,包括中子和质子。它的正电荷来自于带正电的质子。
•质子:它们是原子核中带正电荷的实体,用符号p表示+.
•中子:这些中性的实体存在于原子核内,并负责原子的大多数物理性质。这些用符号n°表示。
•电子:带负电荷的实体,沿固定的圆形轨道绕原子核运动。这些用符号e表示- - - - - -.
电子相对于原子核的位置取决于电子的能量。
•壳:电子绕原子核运动的路径称为壳层或轨道。由于电子的能量和壳层容纳电子的容量不同,只有固定数量的电子被允许沿着特定的轨道运行。
在原子的玻尔模型中,壳层被命名为K、L、M、N等,或者1,2,3,4等。这个数在远离原子核的地方增加。电子的能量也随着壳层数的增加而增加。这就是为什么壳层也被称为能级。
因此,位于k壳层(即最靠近原子核的壳层)的电子被称为处于基态,携带的能量最小。
位于最外层的电子携带最大能量,也称为价电子。这些电子负责成键。
当电子获得能量时,也允许它们从低能级跳跃到高能级,或者当它们失去能量时,从高能级下降到低能级。
氩原子含有22个中子,18个质子和18个电子。电子在K、L和M壳层中围绕原子核旋转。
| 氩原子 | 价值 |
| 不。的质子 | 18 |
| 不。中子 | 22 |
| 电子数 | 18 |
| 炮弹数量 | 3. |
| 第一(K)层电子数 | 2 |
| 第二层(L)电子数 | 8 |
| 第3 (M)层电子数 | 8 |
| 价电子数 | 8 |
氩气玻尔模型的绘制
氩是一种稀有气体,位于元素周期表的第18族:
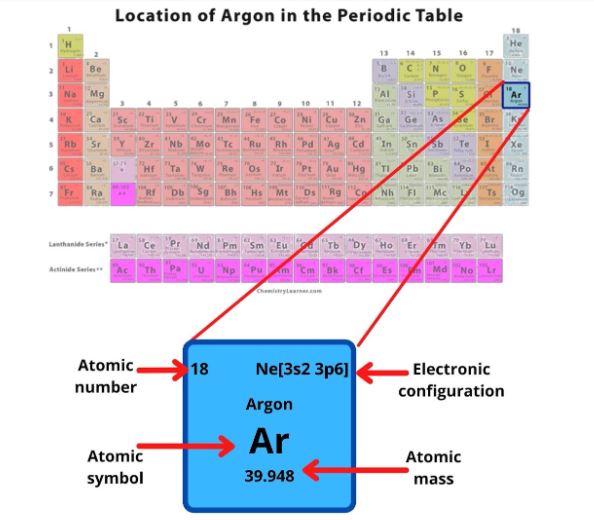
从上述氩气箱中我们可以得到的信息如下:
氩的原子序数是18。
•氯的电子构型是[Ne] 3s23 p6.
•氯的化学符号是Ar。
氯的相对原子质量是39.948。
现在,利用上述信息,我们将绘制氩原子的玻尔原子模型。
为此,我们首先要计算原子的种类。让我们从质子开始。
任何原子的质子数总是等于该原子的原子序数。
氩原子的原子序数是18。
因此,对于氩原子,质子数=原子序数= 18
继续,我们现在要计算氩原子中的中子数。
计算原子中中子数的公式如下:
中子数=原子质量(四舍五入到最接近的整数)-质子数
现在,根据氩盒子里的信息,我们知道氩的相对原子质量是39.948。
四舍五入到最接近的整数后,我们得到40。
同样,根据上面的计算,氩原子中的质子数是18。
现在,把这些值代入上述公式:
中子数= 40 - 18 = 22
因此,氩原子中的中子数= 22
由于质子和中子构成原子核,利用上述数值,我们现在可以画出氩原子的原子核。具体如下:

在这个图中,p+代表质子,n°代表中子。
现在,继续往氩核中加入壳层,我们将计算电子的数量。
对于任何原子,电子数总是等于该原子的原子序数。
因此,对于氩原子,
电子数=氩原子序数= 18
此外,我们现在将计算壳层的数量,以及每个壳层中可以容纳的电子的数量。如前所述,一个特定的壳层中只能容纳有限数量的电子。
某一壳层所能容纳的最大电子数由2n给出2式中,n为壳层数。
现在,将这个公式应用于氩原子,我们将分别计算每个壳层的电子数。
对于氩原子的K壳层,最大电子数= 2 (1)2= 2
把这两个电子加到第一能层后,原子的结构如下:
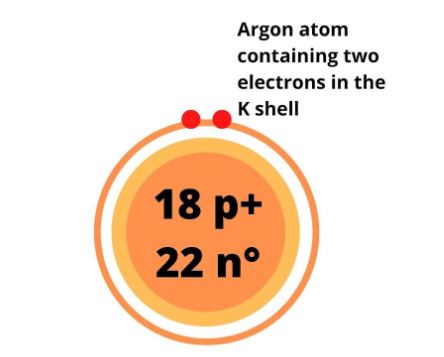
在这之后,电子就会被加到氩原子的L壳层。
让我们计算一下能容纳在L壳层的电子数。
氩原子L壳层的最大电子数= 2 (2)2= 8
因此,L能层能容纳8个电子。
在这个阶段要提到的重要一点是,对于K壳层,只有两个电子彼此靠近。然而,从L壳层开始,随着电子数的增加,排列模式发生了变化。
电子现在按顺时针方向排列成4个一组。前四个电子彼此呈90°。这个角度随着电子数的增加而减小。
因此,氩原子L壳层的前四个电子排列如下:

剩下的4个电子现在又以顺时针的方式加入了L壳层。
在此之后,氩原子现在表示为:
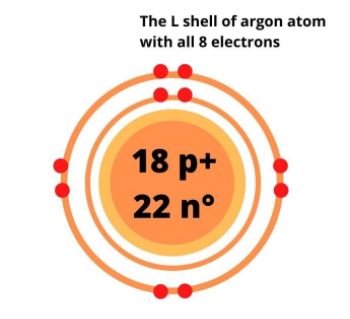
现在,我们还剩下8个电子它们都在M层。
因此,我们将计算能容纳在M壳层的电子数。
氩原子M壳层的最大电子数= 2 (3)2= 18
因此,总共有18个电子被允许容纳在M壳层中。
由于氩原子只剩下8个电子,我们可以把它们都放在M壳层中。
前四个电子再次以顺时针的方式加入。

最后,在把所有8个电子都加到M壳层之后,我们得到了氩原子的玻尔模型,如下图所示。
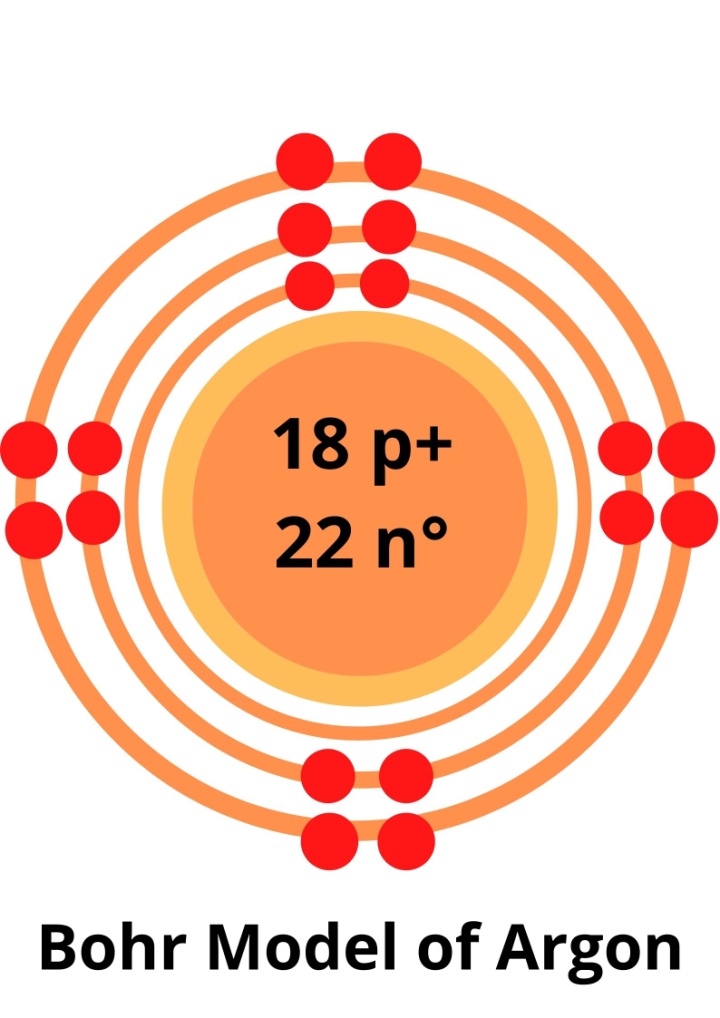
因此,氩原子的最终玻尔模型包括原子核内的18个质子和22个中子,以及围绕原子核旋转的18个电子。
K层有2个电子,L层有8个电子,M层有8个电子。
由玻尔模型推导氩的Lewis结构
路易斯结构或电子点结构是一种元素的原子及其价电子的图解。原子核用元素的原子符号表示,而电子用圆点表示。
如上所述,氩原子由8个电子组成在它的价层即M层。因此,氩的Lewis结构表示如下:
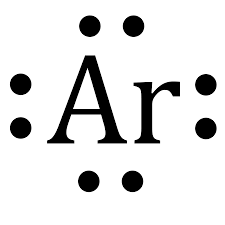
氩的性质
氩的几个重要性质如下:
•它是拉姆齐爵士在1894年发现的。
•它是一种无色气体,在电场的作用下呈紫色。
•氩的熔点和沸点分别为−185.848°C和−189.34°C。
•氩的密度为1.78.103g.cm3在0°C。
•氩在水中的溶解度与氮相似,是氮的2.5倍。
下面是氩气玻尔模型的视频。
相关的话题
结论
根据玻尔原子模型,氩原子由18个质子和22个中子组成,18个电子围绕原子核旋转。
一个原子中的质子数和电子数总是等于这个原子的原子序数。
中子数由公式给出:
中子数=原子质量(四舍五入到最接近的整数)-质子数
一个壳层所能容纳的最大电子数由公式2n给出2,其中n为壳层数。
氩原子由三个壳层组成,K、L和M壳层分别有2个、8个和8个电子。
快乐学习! !