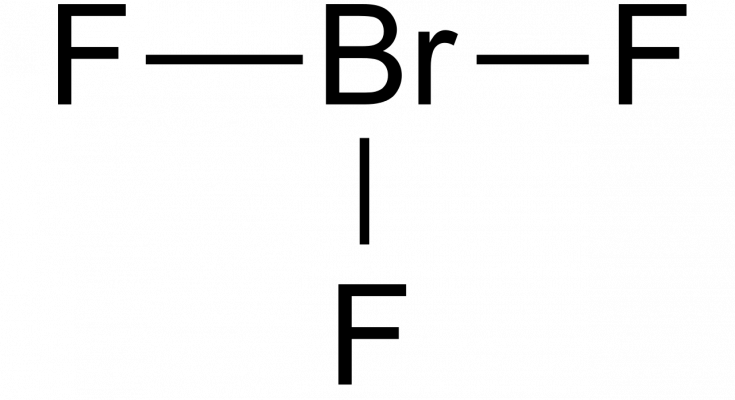BrF3,被称为三氟化溴,是一种由卤素间组合组成的发烟液体,具有刺激性气味。
这种化合物有一种吸管,即无色到黄色的外观,有多种应用,但也有一些局限性和危险问题。
以下是我们如何合成或制备化合物BrF3:

由于BrF3由三个氟分子组成,这是一种强氟化剂。同时含Br和F,可产生HBr和HF酸。
三氟化溴的一些特性是易溶于硫酸和作氟供体。
不仅如此,它在火箭推进剂中作为氧化剂,以及作为强大的无机溶剂,甚至在制造用于核燃料的铀组合卤素中也有应用。
BrF3的广泛用途并不能否定这样一个事实,即BrF3在水中具有高度活性,并具有相当的毒性,可导致不同的人类疾病,从皮肤烧伤到眼睛溃疡和呼吸系统刺激。
BrF3中的化学键合
从核心彻底了解任何化合物的关键是通过它的结合性质和强度。如果我们能够了解为什么某些原子相互靠近并结合形成复杂的化学结构,以及它们形成的不同类型的化学键来达到这种复杂性,并形成更大的化合物,就能理解任何给定分子或离子的化学键。
我们有不同类型的化学键:离子键、共价键、金属键、氢键等等。在不同的分子中我们有不同的键强度和反应性。
我们已经看到了导致不同化学成分的独特排列,这些化学成分表现出对比或相似的化学和物理性质。
BrF3作为一种卤间化合物,由于其独特的成键性质,具有独特的特性和反应强度。
在这里,在这篇文章中,我们将尝试建立一些关于三氟化溴分子内部发生的键的知识。
要做到这一点,我们必须首先学习为BrF3描绘一个完美的刘易斯结构的步骤。
BrF3 Lewis结构
定义
分子形成时,是由几个相同或不同的原子元素聚集在一起,形成单键或多键,形成上述分子结构。
刘易斯结构是在构成元素、价电子概念和键的形成的帮助下,给予任何分子组成或离子骨架的图解形式。
这是一个二维结构表示,给了我们一个简短而清晰的概念,关于分子的内部位置。
形成BrF3 Lewis结构的步骤
步骤1:一个BrF3分子含有多少价电子?Br和F都是元素周期表中第7族的卤素。
因此,这两个元素的价电子都是7。BrF3中价电子的总数
= 7 + 7*3
= 7 + 21
= 28。
步骤2现在,哪个原子会充当中心原子呢?
根据一般规则,我们把电负性最小的元素放在中间。
电负性图显示溴的电负性值为2.96,而F的电负性值为3.98。
因此,我们把唯一的Br原子放在中间,两边是F原子。
步骤3现在,我们将把28个价电子放在原子周围,以实现八隅电子的满足。
我们已经实现了这里每个原子的八隅结构。Br和3个F原子都有8个电子作为价电子围绕在它们周围。

步骤4溴和每个氟原子会形成一个单键。但是,如果我们计算总数,它会数到26而不是28。
步骤5我们现在该怎么办?
我们把电子对放在溴的上面。这是八隅体规则的一个例外Br周围有10个价电子。

步骤6:为了检验这是否是BrF3最合适的Lewis结构形式,我们必须了解另一个概念:形式电荷。
形式电荷是赋予化学分子内组成原子的电荷,其中键在所有存在的原子中平均共享。
这就是我们计算形式电荷的方法。

在路易斯结构形成中,我们必须检查是否所有的原子都有它们可能的最小形式电荷值。
让我们计算BrF3:
F:形式电荷= 7- 0.5* 2 -6 = 0
Br:形式电荷= 7- 0.5*6 -4 = 0
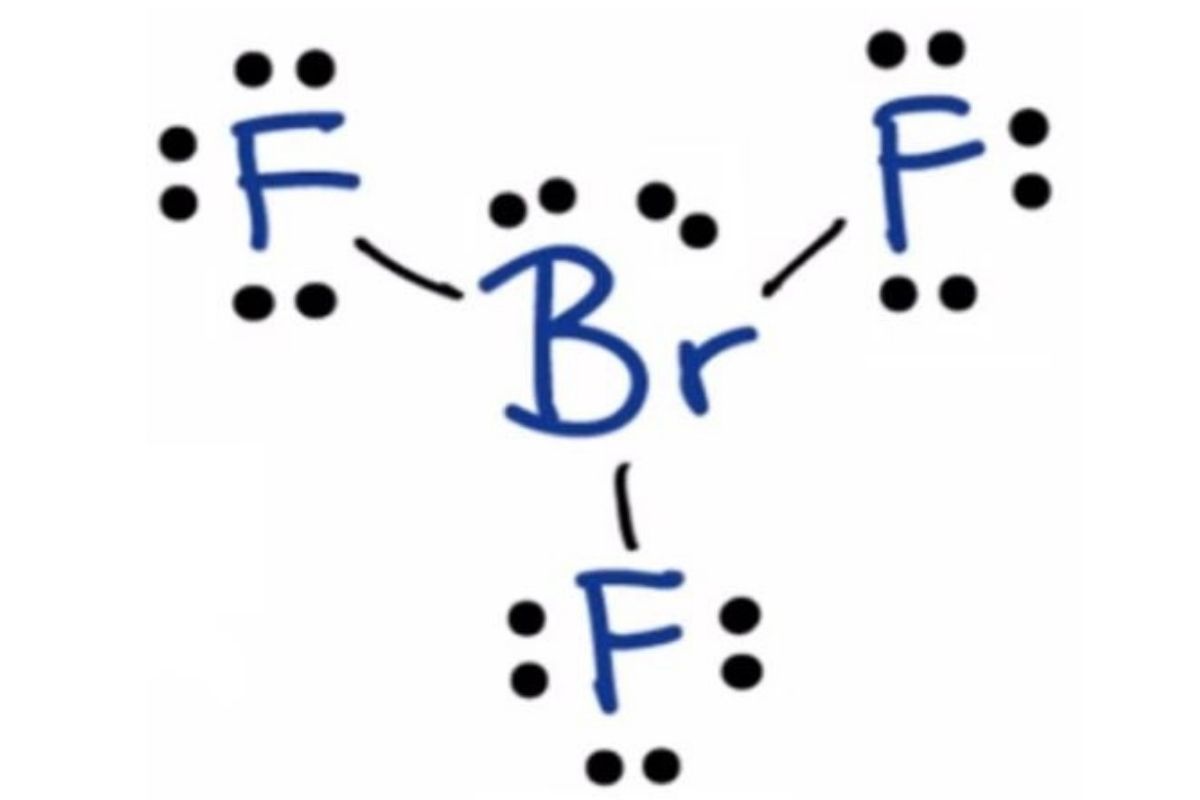
我们可以看到三个F原子和一个Br原子的形式电荷值都是0。因此,我们可以得出结论,我们已经得到了最合适的LS图。
分子几何
什么是分子几何?
分子几何是基于VSEPR理论的一个基本概念,它帮助我们确定分子的三维结构。
VSEPR理论是价壳电子对排斥理论的缩写。
我们用来找出任何给定成分的确切分子形状的模型是一种理论方法,它依赖于电子云类似电荷的排斥性。
你知道分子中围绕原子核的每一个价电子都有一个作用来最小化它们所经历的斥力,这样才能达到平衡的几何结构吗?
电子是共用单键、双键还是三键,甚至是孤对电子,都无关紧要。然而,斥力的强度是不同的-结合对之间的经验最少,而孤独对之间的最大。
现在让我们用这个概念来找出BrF3的分子几何结构。
分子几何
让我们再看一看刘易斯结构。
Br是中心原子。有三个氟原子围绕着中心的溴原子,因此有三个键对。
溴原子上有两个孤对,这是八隅体规则的一个例外。
空间数在这里是一个重要的术语,我们需要找出任何VSEPR计算。
空间数表示成键电子数和中心原子上孤对电子数之和。
BrF3中的空间数= 3+2 = 5
现在让我们看看下面的图表:
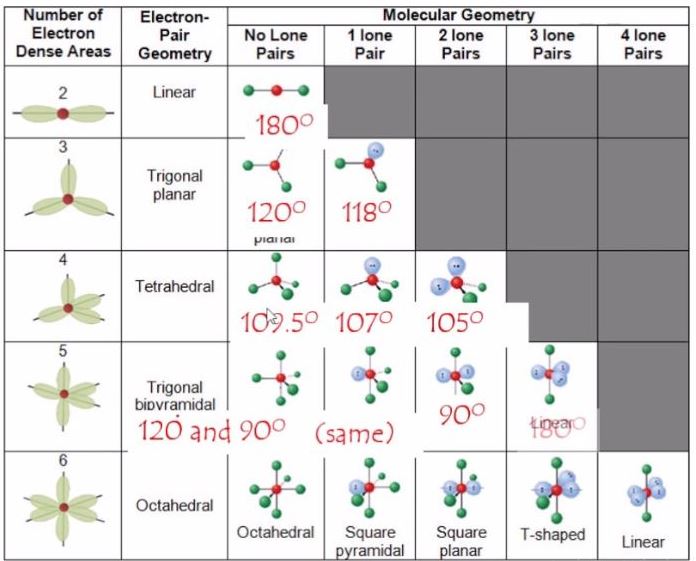
如果我们仔细观察,我们可以指出三氟化溴的VSEPR几何形状是t型的。
如果我们看这个分子类似的字母T,我们可以推断出这个角是90度。
但这里,键角减小到86度左右,小于90度。
这是由于卤素F的高电负性功率,也由于两个孤对的影响,使键的角度小于90度。
因此,BrF3分子是弯曲的t型.

BrF3极性
BrF3分子被认为是非极性分子。
由于Br原子和F原子的电负性有很大的差别。电荷在整个分子中分布不均匀。
由于溴原子上存在孤对,BrF3的形状是不对称的,这也是电荷分布不均匀的主要原因。
这种非极性分子的净偶极矩非零。
有关详细信息,您必须阅读预先写好的文章BrF3的极性.
BrF3杂交
我们还没有正确地破译任何给定的分子化合物的成键性质,除非和直到我们对杂交进行了研究。
简短的介绍
轨道杂化在化学键这一章中是一个不可分割的概念,在化学键这一章中,我们讨论了s, p, d和f等几个原子轨道,以及它们如何结合和聚变产生几个杂化轨道来形成键。
根据组合类型,我们有几个层次的杂交。我们有sp, sp2, sp3, sp3d等等。
BrF3中溴的杂化是什么?
BrF3分子经过sp3d杂交.
让我们看看F和Br的电子排布。
F: 1s2 2s2 2p5
F:[他]2s2 2p5
Br: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5
Br: [Ar] 4s2 3d10 4p5
当我们观察Br和每个氟原子成键时,成对的电子会转移到4d轨道上。
因此我们有一个s轨道,px py pz轨道和一个d轨道(比如dxy)
因此,我们会有sp3d杂化,这个过程也取决于空间位数,我们已经在分子几何部分讨论过了。
分子轨道图
分子轨道理论,用来描绘任何给定分子的MO图,是一个复杂而重要的化学键概念。
在量子力学中,MO理论处理电子的空间和能量性质,并讨论LCAO(原子轨道的线性组合)形成MO(分子轨道)。
它有几种类型的轨道:成键,反键,非成键。除此之外,我们还看到sigma, pi, delta, HUMO和LUMO的概念。
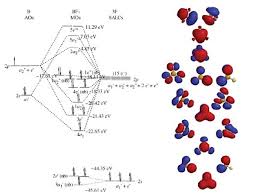
上图为BF3(三氟化硼)的MO结构,供大家参考。
结论
在这篇文章中,我们讨论了BrF3分子的化学键的基本原理。我们讨论了三氟化溴的Lewis结构、分子几何、杂化和MO图。
我希望你喜欢阅读我的文章并获得知识。如果你还有什么问题想问,请告诉我
阅读的快乐!