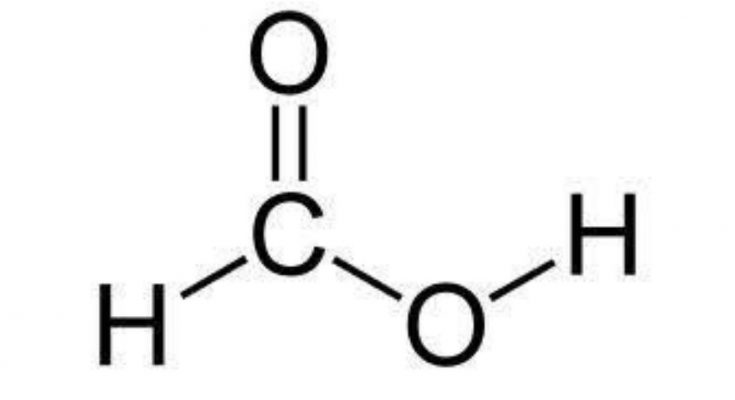
甲酸的化学式是HCOOH或CH2O2,其中一个氢原子连接到-COOH基团上形成最简单的羧酸。万博体育app手机版登录它也被称为甲醇酸。
你知道吗,甲酸可以自然地存在于几种昆虫王国中,如蚂蚁和无刺蜜蜂?
我们在工业中通过以下公式制备HCOOH:
Ch3oh + co—> hco2ch3 (1)
Hco2ch3 + h2o—> hcooh + ch3oh (2)
在实验室制备中,必要的化学反应是:
C2o4h2—> co2h2 + co2
同时,
Pb(HCOO)2 + H2S—> 2HCOOH + PbS
甲酸的分子量为47.018 g/mol,密度为1.220 g/ml。它是一种无色的发烟液体,带有刺鼻的穿透性气味。
它被用作燃料电池,也作为反相高效液相色谱方法的流动相的组成部分。
除此之外,HCOOH还可用于皮革生产和染色工业,作为杀菌剂和抗菌剂。
现在让我们学习一下这种羧酸化合物的化学键。
C万博体育app手机版登录H2O2 Lewis结构
如果我们想找出任何多原子分子内部化学键的本质,我们需要画出路易斯结构。
路易斯结构给了我们一个一步一步的步骤来描绘一个给定分子的二维示意图表示。在这里,我们用价电子的概念来找出键的形成类型。
在甲烷酸中,有两个氢原子,一个碳原子和一个氧原子。
这是现代元素周期表的图片。
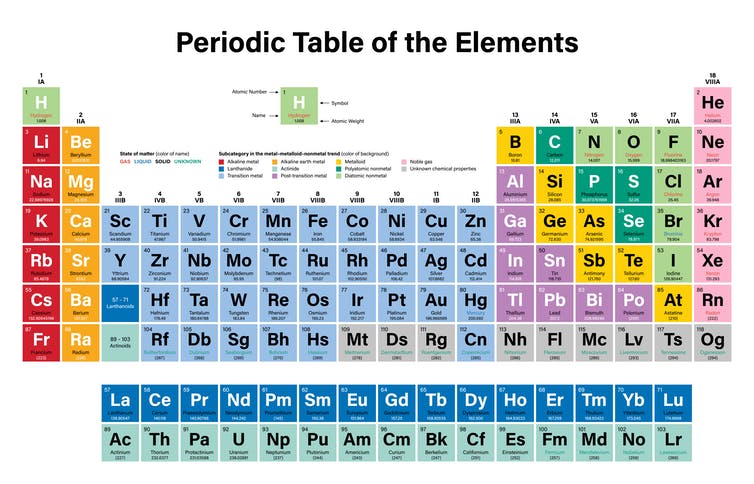
我们可以看到,碳的价电子是4,有4个价电子。氧属于第16族(硫族),有6个价电子。
氢属于第1族,最外层只有1个电子(价电子)。
价电子总数= 1*2 + 4*1 + 6*2 = 18。
在三种元素中,氢的电负性值最小,碳次之,氧的电负性值最高。
根据一般规律,电负性最小的元素必须占据中心位置。
然而,由于氢原子只有一个价电子,它倾向于停留在角落,而不是成为中心原子。
所以甲酸的中心原子是碳。
原子看起来是这样的:

现在,我们把价电子放在每个组成原子的周围,图会是这样的:
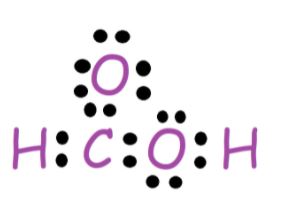
这里有一个非常必要的概念:八隅规则。根据这一规律,在1-17组(主要基团)中存在的每一个元素都倾向于在价壳层中获得像惰性气体元素那样的八隅体构型。
例如,氮倾向于有氖构型而氯倾向于有氩构型。
你可能听说过化学中有很多例外,其中一个例外就是氢倾向于达到氦的构型,因此总共需要2个电子来满足价层。
在上图中,我们可以注意到碳还没有达到八隅体完满状态。为了做到这一点,我们将在原子周围多带两个电子。
所需草图如下:
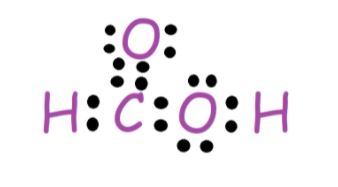
如果我们计算形式电荷:
这是求形式电荷值的公式:

C的形式电荷= 4 - 0.5*8 - 0 = 0。
形式电荷为H = 1 - 0.5*2 - 0 = 0。
O与H和C成键的形式电荷均为6 - 0.5*4 - 4 = 0。
O与C键合的形式电荷= 6 - 0.5*4 - 4 = 0。
因此,原子以它们最不正规的电荷值存在。
最适合甲醇的Lewis结构为:

C万博体育app手机版登录H2O2分子几何
VSEPR是价壳电子对排斥理论的缩写。该模型在化学中用于从给定成分的刘易斯结构预测其分子几何结构。
Lewis结构为我们提供了化学分子的二维表示,VSEPR模型为我们破译三维分子形状提供了基础。
这与共价键分子有关。它考虑了电子对(包括成键电子对和未成键电子对),并讨论了最小斥力的概念。
根据VSEPR理论,电子在原子核周围形成一个带负电的气氛,这就在同类电荷之间产生了排斥力。
分子的稳定性是通过增加电子之间的距离来维持的,从而使排斥力最小化。
在VSEPR理论中,我们可以通过VSEPR符号来预测分子的几何形状。
AXnEx是VSEPR符号。
这里,A代表中心原子,X代表周围原子(在VSEPR中,我们也认为三键和双键是一个键基),
E表示连接在中心原子上的孤对数。
这里,碳是中心原子(A)。X: 2个氧原子和1个氢原子,
∴n = 3。
E:没有孤对A,∴x = 0。
AX3E0是甲酸的VSEPR符号。
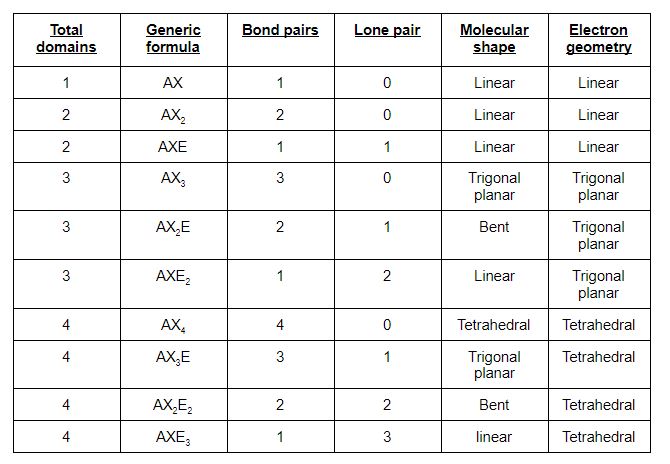
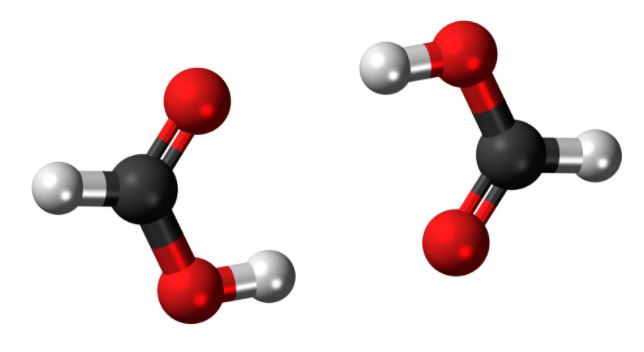
从图表中我们可以看到,HCOOH的分子几何形状为三角平面。
C万博体育app手机版登录H2O2杂交
轨道杂化是描述化学键性质的重要模型之一。
杂化的概念涉及原子轨道(AOs)。具有等效能量的同一原子的轨道聚集在一起,结合和聚变,形成杂化轨道。价层电子参与其中。这些杂化轨道被认为参与了化学键的形成。
现在,让我们解读一下甲醇的杂化类型。
空间数=分子内与中心原子结合的原子数+与中心原子结合的孤对电子数
在HCOOH中,中心原子碳与一个氧原子成双键,与另一个氧原子和一个氢原子成单键。
甲酸中没有孤电子对或未成键电子对。
∴空间数= 3 + 0 = 3。
所以碳有sp2杂化。
对于碳氧轨道的氧,我们有sp2杂化,因为它有两个孤对和一个成键原子而碳氧轨道的氧,我们有sp3杂化,因为有两个孤对和两个sigma键。
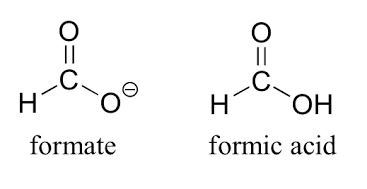
C万博体育app手机版登录H2O2极性
现在让我们谈谈极性。
极性是化学分子的一个重要特征或性质。它与分子内部组成原子间的电荷分布有关。
什么时候可以称分子为极性分子?当电子在原子间的分布不均匀时,即在分子组成中存在不对称的电荷分布时,我们可以将分子称为极性分子。
我们可以从电负性的概念来检验。两个原子元素之间的电负性在0.4 - 2之间的差异被认为是极性共价键。
这里是鲍林电负性图:
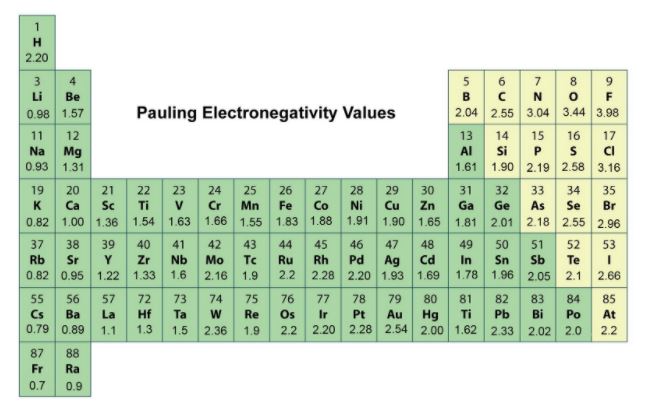
在C-H键中,差值为2.55 - 2.20 = 0.35。
在C和O键中,差值为3.44 - 2.55 = 0.89。
在O-H键中,差值为:3.44 - 2.20 = 1.24
正如我们所看到的,化学键倾向于极性。与此同时,我们有一个不对称的结构氢的一端在正极而氧的一端在负极。
HCOOH本质上是极性的。在水和极性有机溶剂中可混溶。
结论
羟基羧酸是最简单的羧酸,是一种重要的有机分子。我们在本文中详细讨论了化学键。
学习快乐!