CH3NH2是甲胺的分子式,甲胺是最简单的胺。由此,很明显,这个分子有一个有孤对的基本氮原子。甲胺是一种有机分子,气态无色,是氨的衍生物。
此外,该分子具有强烈的刺鼻鱼腥味,商业上用于生产麻黄碱、呋喃、甲基苯二甲酸钠、甲酰胺甲酯、茶碱、西巴威、n -甲基吡罗烷酮。甲胺是一种已知的亲核试剂,它通过提供电子对与亲电试剂成键,这使它成为路易斯碱。
路易斯碱是一种供体分子,它很容易提供一对非成键电子来实现稳定的电子构型。
甲胺(CH3NH2)的Lewis结构
路易斯结构是价电子如何运动以确保键的形成的图解表示。要研究一种化合物,路易斯结构是第一步,因为它有助于确定分子属于元素周期表中的哪个基团。
它是一种有利于共价化合物的性质,主要用于研究参与原子上的形式电荷和原子之间发生的化学键。当一个分子可以画出多个刘易斯图时,这些图被称为共振结构。
首先,要了解甲胺(CH3NH2)的刘易斯结构,首先要了解每个参与原子有多少价电子。碳的电子排布是1s2 2s2 2p2,因为它的原子序数是6。
由于p壳层最多能容纳6个电子,因此有4个电子的空位形成了碳4的价电子。此外,氢和氮的原子序数分别为1和7,电子排布分别为1s1和1s2 2s2 2p1。
由于s壳层可以容纳2个价电子,p壳层可以容纳6个以稳定它们的八隅体,氢的价电子为1,氮的价电子为5。
现在,让我们研究绘制甲胺(CH3NH2)刘易斯结构的步骤:
步骤1:求甲胺的价电子总数:对于一个甲胺(CH3NH2)分子,它是14,因为4个来自碳原子,1个来自氢原子,5个来自氮原子。
步骤2:求出一个甲胺(CH3NH2)还需要多少价电子一个甲胺(CH3NH2)分子需要12个价电子,因为每个氢原子需要1个价电子,碳原子和氮原子需要4和3个价电子。
步骤3:寻找一个甲胺(CH3NH2)分子的中心原子:从分子式中可以清楚地看出,三个氢原子与碳原子结合,而两个与氮原子结合.这使得CH3和NH2成为两个独立的实体,产生两个中心原子,即碳和氮。
步骤4:找出甲胺(CH3NH2)原子间成键的方式:由于甲胺(CH3NH2)是一种胺,参与的原子之间形成单键,氮原子上有一对孤电子。
步骤5:现在,通过分析前面提到的各个点,画出结构:
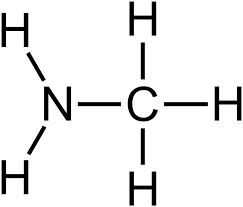
甲胺(CH3NH2)的分子构型
分子的分子几何结构取决于刘易斯结构,并有助于确定键长、角度、类型和其他基于每个参与原子的位置的几何参数。
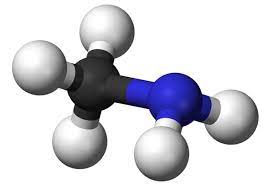
由于甲胺(CH3NH2)中有两个中心原子,两者的分子几何形状将因键角不同而不同。以-CH3为主要目标的碳,其分子几何形状为四面体,成键角为109.5°。而氮气靶向-NH2端时,其分子几何形状为三角锥体,键角约为108.9°。
如果你意识到三角锥体形状的理想键角是109.5°,那么这个偏离理想百分比的偏差可以用氮原子上孤对电子的存在来解释。
这可以用价层电子对斥力(VSEPR)理论来解释,该理论认为孤电子对存在于比有成键电子对的轨道更短更圆的轨道中。
这导致孤电子对和成键对之间的过度排斥,使键角从理想百分比降低。
甲胺(CH3NH2)杂化
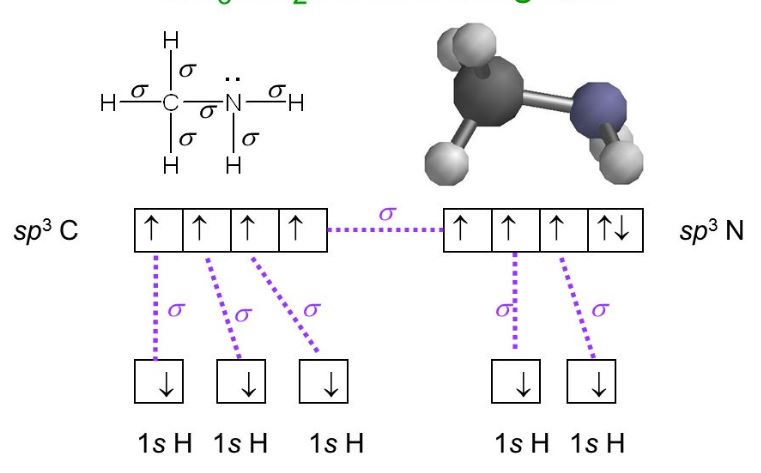
杂化是一种理论观点,它认为原子轨道以某种方式混合和重叠,形成新的杂化轨道,从而影响整个分子的几何结构和参与原子的化学键性质,从而改变整个分子。
这种混合和重叠的发生符合量子力学的原理,即能量相似的原子轨道可以参与杂交过程,包括充满轨道和半充满轨道。
根据价电子键理论(VBT),可以分析出甲胺(CH3NH2)中的碳原子和氮原子都是sp3杂化的,因为C-N sigma键在两个sp3轨道之间重叠。
Sp3杂化意味着中心原子有小时Sp3杂化轨道。两个sp3杂化轨道重叠并与氢原子的s轨道混合产生两个N-H键。
一个sp3杂化轨道与碳原子的sp3杂化轨道重叠并混合形成一个C-N键。第四个杂化轨道由氮原子的孤对电子组成。
甲胺(CH3NH2)的极性
化学分子的极性是一种性质,使它们能够决定是否吸引附近的原子。化学极性导致电荷的分离,通过形成一个带正电的一端和另一个带负电的一端,在分子上产生一个整体的净偶极矩。
分子的极性可以很容易地通过参与原子的电负性值来研究。这是原子为了稳定电子构型而吸引共用电子对的一种趋势。
电负性的大小取决于价电子的数目和它们到原子核的距离。价电子的数量越多,吸引电子的趋势就越大,电负性值也就越高。
然而,价电子的数量越少,吸引电子的趋势就越低(它们会被捐赠),电负性值也就越低。
当谈到甲胺(CH3NH2)时,它是一个极性分子,因为参与原子之间的电负性差异,整个分子上存在偶极矩。碳、氢、氮的电负性分别为2.55、2.20、3.04。
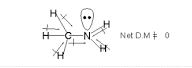
在碳氮成键的情况下,偶极矩会向氮移动,因为氮的电负性值较高。而在氮和氢键的情况下,由于氮原子上存在孤对,偶极矩再次被加起来,偶极矩向上移动,也就是氮原子的方向。
由于氮原子本身具有最高的电负性值,偶极矩将在它周围最高,这将导致在甲胺(CH3NH2)分子中的极性。
此外,由于碳原子和氢原子之间的差异很小,几乎可以忽略不计,所以这个键在本质上是非极性的,但它的强度远小于氮原子周围的偶极矩。因此,甲胺(CH3NH2)是一个极性分子。
结论
甲胺(CH3NH2)是一种亲核试剂,也是已知的最简单的胺,这使得它成为键形成的良好电子供体。刘易斯结构有助于发现甲胺分子有两个中心原子,使分子几何结构为四面体和三角锥体。
此外,两个中心原子都是sp3杂化的,碳原子的键角符合理想百分比,而氮原子的键角由于孤对电子的存在而出现偏差,且键角数低于预期。
最后,甲胺分子本质上是极性的,因为氮原子上的偶极矩很高,而碳-氢键上的偶极矩可以忽略不计。




