CH3OH是甲醇的分子式,又称甲醇,是最简单的脂肪族醇。它是一个甲基与一个羟基官能团相连的伯烷基醇。
由于羟基官能团的存在,它是一种极性溶剂。它的分子质量为32.042g,无色,具有刺激性气味和挥发性。
要更多地了解甲醇,有必要了解它的成键特性。
为此,需要详细了解Lewis结构、VSEPR理论、杂化概念及其极性性质。
CH3OH Lewis结构
分子的路易斯结构给出了分子周围价层电子的最简单表示。
在这里,价电子用小点表示,由于单键由两个成键电子组成,两个原子之间的两个点用一条线表示,这条线表示它们之间的键。
刘易斯结构给了我们关于原子间存在键的信息,尽管它还不足以告诉我们键的类型。
为了建立甲醇的路易斯结构,首先要满足八隅体规则,然后计算分子中每个元素的形式电荷。
八隅体规则规定,每个元素获得惰性气体构型,即共有2个电子(在H和He的情况下)或在它们的价壳层中共有8个电子。这是因为惰性气体在自然界中被认为是稳定的。
形式电荷是存在于分子元素上的理论电荷。这些形式电荷的和必须等于分子上的净电荷。计算公式如下:
元素的形式电荷=(价电子)-(成键电子)/2 -(非成键电子)
甲醇(CH3OH) Lewis结构的绘制步骤
1)甲醇总价电子的计算
完全没有。分子中价电子的总和是分子中每个元素的价壳电子的总和。
看看下面的表格。
| 原子 | 原子序数 | 组数 | 电子配置 | 价电子层电子配置 | 不。的价电子 |
| C | 6 | 14 | 1 s22s22p2 | 2 s22p2 | 4 |
| O | 8 | 16 | 1 s22s22p4 | 2 s22p4 | 6 |
| H | 1 | 1 | 1 s1 | 1 s1 | 1 |
现在,一个CH3OH分子中有1个碳原子,1个氧原子和4个氢原子。因此总价电子为:
(1*4) +(1*6) +(1*4) = 14个价层电子
2)草图
为了画一个粗略的草图,需要选择分子的中心原子。
中心原子的电负性不能很强,体积也不能太小。因此,在甲醇中,C和O都是合适的中心原子。
但是,只要把这两种元素中的任何一种看作中心原子,就可以很容易地画出甲醇的路易斯结构。
在这里,我们将进一步以碳原子为中心原子。我们可以观察到,甲醇有三个C-H键,一个C-O键和一个O-H键。
粗略的草图如下图所示。

3)将价电子放置在单个原子周围
下面说明了价电子是如何分布在各自原子周围的。

4)满足每个原子的八隅体规则,画出最终的路易斯结构
由于甲醇共有14个价壳电子,因此,分子中必然有7对电子对。
我们知道两个成键电子在一起形成一个键用一条线表示。
下面的图像显示了路易斯结构,它有所有的键和孤对可见,并满足八隅体规则。

为了完成路易斯图,最后一步是计算形式电荷。正如我们之前讨论的计算形式电荷的公式,它可以这样做;
元素的形式电荷=(价电子)-(成键电子)/2 -(非成键电子)
在那里;
成键电子是参与成键的电子。
非成键电子是围绕在每个原子周围的不参与成键的孤对电子。
| 原子 | 价电子 | 成键电子 | 孤对电子电子 | 形式电荷 |
| C | 4 | 8 | 0 | 0 |
| O | 6 | 4 | 4 | 0 |
| H | 1 | 2 | 0 | 0 |
一个分子上的净电荷是每个原子上形式电荷的总和。因此,甲醇分子上的净电荷为;
(1*0) c + (1*0) o + (4*0) h = 0
这意味着甲醇是一种中性化合物,在氧原子上有两个孤对,其最终的刘易斯结构如下图所示;
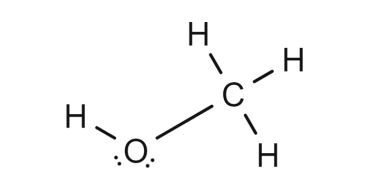
然而,Lewis结构给出了关于某种化合物的许多信息,这是令人满意的,尽管很难通过这个概念准确地说出化合物的几何结构和杂化。
因此,有必要了解VSEPR理论和杂化概念。
CH3OH分子几何
化合物的分子几何结构可以很好地用价层电子对斥力(VSEPR)理论来解释,该理论基于这样一个假设,即分子将自身稳定在一个特定的形状中,在这个形状中,它经历了最小数量的电子-电子斥力。
一个分子的分子形状与其分子几何形状是不相同的。键对中的电子,空间位姿数不为零,即分子中含有非零孤对。
立体数是根据VSEPR理论分配给每种几何类型的一个特定值,可通过以下公式计算:
空间数(S) = (X + M + |a| - b)/2
在那里;
X = no。中心原子的价电子
M = no。单原子侧原子
A =分子上的负电荷
B =分子上的正电荷
下表显示了分配给每个几何的空间数。

根据VSEPR理论计算CH3OH的空间位数如下:
1)计算以碳为中心原子的甲醇的空间位数。
●没有。碳原子的价电子是4
●没有。单原子侧原子= 4
根据形式电荷计算,甲醇是中性的,因此a和b的值为0。
CH3OH的空间空间数wrt C = (4 + 4) / 2 = 4
由于甲醇分子的空间位数是4,这意味着它相对于碳原子具有四面体几何结构。
2)计算以氧为中心原子的甲醇的空间位数。
●没有。氧原子的价电子是6
●没有。单原子侧原子= 2
根据形式电荷计算,甲醇是中性的,因此a和b的值为0。
CH3OH的空间位阻数wrt O = (6 + 2) / 2 = 4
由于甲醇分子的空间位数是4,这意味着它相对于氧原子也是四面体几何。
CH3OH分子形状
具有四面体几何结构的化合物可以有四种类型的分子形状,这取决于否。分子中存在的孤对。
由于分子中存在孤对-孤对排斥、孤对-键对排斥和键对-键对排斥,某种特定几何类型中的各种形状就会发生。
没有。化合物中孤对的数量可以通过减去no来计算。空间位数的键对。
●如果一个化合物有3对键对和1对孤对,那么它将呈金字塔形。
●如果一个化合物有2个键对和2个孤对,那么它就会有弯曲的形状或线性形状。
●如果一个化合物有4个键对而没有孤键对,那么它就是四面体几何结构。
因此,以甲醇为例;
●由于中心碳原子有4 sigma键,没有孤对,这意味着甲醇相对于碳原子具有四面体形状,键角相等,为109.5度。
●由于氧原子有2个sigma键和2个孤对,这意味着甲醇相对于氧原子具有弯曲的形状,键角为104.5度。

CH3OH杂交
杂化是描述能量和形状相同的纯原子轨道混合形成杂化轨道的概念。
然而,有必要不。这样形成的杂化轨道的总能量必须等于no。混合在一起的原子轨道。
杂化概念有助于解释化合物几何形状上的成键。
例如,杂化可以很容易地或直接地从化合物本身的空间位数来计算。
下表显示了每个空间数值各自的杂化。

从表中我们可以看出,甲醇对以碳和氧为中心原子的杂化反应是sp3 wrt,因为它们都使分子的空间位数等于4。
另一方面,计算化合物杂化的详细方法如下:
C在基态下的电子构型为1s2 2s2 2p2,表示为
如下:

为了与三个氢原子和一个羟基结合,碳需要将2s轨道上的一个价电子激发到2p轨道上,从而扩展八隅体。
激发态碳的电子排布是1s2 2s1 2p3表示为
如下:

四个原子轨道;1个2s轨道和3个2p轨道相互混合形成4个sp3杂化轨道,如下图所示。

因此,我们可以说CH3OH的杂化轨道是sp3轨道。
我还写过一篇关于乙醇的文章。去看看乙醇的杂化,几何和路易斯结构.
CH3OH极性
如果两个原子之间的电荷分布不相等,或者它们之间存在电负性差异,则两个原子之间的键称为极性键。
另一个决定化合物极性的因素是偶极矩,它是原子的部分电荷和它们之间的距离的乘积的大小。
如果偶极矩(μ)不为零,即μ≠0,则称任何化合物为极性化合物。
为了使偶极矩存在于两个原子之间,它们之间需要有一个电负性差。
我们知道甲醇有三个碳氢键,一个碳氢键,一个氧氢键。
所以我们需要计算碳氧键,碳氧键和氧氧键之间的电负性差。
C的电负性为2.55,O为3.44,H为2.2。
●C-H键的电负性差为2.55 - 2.2 = 0.35,几乎可以忽略不计。所以碳氢键是非极性的。
C-O键的电负性差为3.44 - 2.55 = 0.89,不可忽略。所以碳氧键是极性的。
O-H键的电负性差是3.44 - 2.2 = 1.24,这使得这个键是极性的。
现在,通过观察图像,我们可以看到描绘偶极矩方向的两个箭头都指向氧原子。
这是因为氧相对于碳或氢具有更强的电负性(从电负性值可以看出),所以键的电子密度更多地向氧移动,因此两个偶极矩不会相互抵消。
有关更详细的信息,您必须查看CH3OH的极性.

这意味着甲醇是极性分子。
然而,众所周知,甲醇在许多化学反应中用作极性溶剂。
这是由于羟基官能团的存在,导致化合物中的氢键。
当甲醇分子溶解在水中时,羟基的存在启动了甲醇分子和水分子之间的氢键。
这使得化合物可溶于水。
结论
综上所述,CH3OH是一种极性和中性化合物,具有四面体几何结构,以及相对于氧原子和碳原子的弯曲和四面体形状。
它有三个C-H非极性键,一个C-O极性键,一个O-H极性键还有sp3杂化。




