阳离子H3O+被称为水合氢离子。如果我们看到水合氢离子的命名法,就会知道根据IUPAC命名法,水合氢离子可以被称为氧离子。
氧离子是所有三价氧阳离子的通称,所以使用水合氢离子这个名称是有必要的,特别是用来区分水合氢离子。
水合氢离子的摩尔质量是19.02 g/mol。
这种离子是在水的质子化过程中产生的;
H2O(水)+ H+(氢离子)—> H3O+
这种离子被用来测定水的pH值。当水分解成OH-和H3O+时,我们可以用特定的方法来检查水的pH值。
水合氢离子用于各种反应和不同化合物的生产。有机化学和无机化学在很大程度上都包含水合氢离子。
但是在阅读这种离子在不同反应中的应用之前,我们必须了解这种离子的基本知识,比如路易斯结构、几何等等。
了解这些基本知识将加深我们对这种离子的认识。在研究任何化合物的反应之前,我们都应该了解它的背景。
所以让我们深入挖掘,了解一些关于水合氢离子的有趣信息!
H3O+ Lewis结构
让我们试着画出H3O+的路易斯结构。
首先,我们需要计算水合氢离子中价电子的总数。
氢= 1
3*氢= 3
氧气= 6
总数= 9
重要的一点是,不要忘记加号。+表示从总价电子中失去一个电子。
(-表示得到一个电子)
因此,总价电子现在是8。
其次,我们需要确定一个中心原子,这个原子通常具有最多的成键位点。在这种情况下,氧原子是中心原子。
接下来,我们需要画出只有单键的H3O+的骨架结构。在那之后,为了完成H3O+的路易斯结构,我们必须用剩余的电子填满原子的八隅体。
在画出H3O+的路易斯结构的最后,我们应该检查一下,所有的原子都有它们可能的最低形式电荷。
下面的附图显示了水合氢离子的刘易斯结构;

如何画路易斯结构
刘易斯结构有助于我们了解化合物的结构、类型、键的数量、物理性质以及化合物如何与其他化合物相互作用。
画一个路易斯结构非常简单!
有一种常用的方法可以画出任何化合物的路易斯结构。为了简化这个过程,我把下面的步骤用圆点表示出来:
- 计算分子中价电子的总数。计算时一定要注意+号和-号。
- 选择一个中心原子;通常是键位最高的原子。
- 画一个只有单键的骨架结构。
- 用剩下的电子填满原子的八隅体。记住,从带电负性的原子开始,再到带电正性的原子。
- 如果需要,给出多个键来完成原子的八隅体。
- 最后,确保所有原子的形式电荷都尽可能低。你可以用下面的公式来计算:-

刘易斯结构规则几乎对所有分子都是一样的,尽管这里也存在一些例外。毕竟化学都是关于例外的!!
H3O +杂交
H3O+(水合氢离子)的杂化为Sp3。
任何分子的杂化都可以用公式求出来。
H = 1 / 2 [v + m-c + a]
在这里,
H =杂交
V = No。价电子的
M = no。单价原子的
C=阳离子的电荷
负离子的电荷
若,H= 2 = Sp杂化
H= 3 = Sp2杂化
H= 4 = Sp3杂化
H= 5 = Sp3d杂交
H= 6 = Sp3d2杂化
现在我们用这个公式来求H3O+的杂化轨道,
在水合氢离子中,中心原子是氧原子它有6个价电子。
根据公式,V = 6
3个氢原子与氧原子成键,所以单价原子的数量(M) = 3
因为这是一个阳离子分子,所以C = 1
所以,H = 1 / 2 [6 + 3 - 1] = 4
因此我们可以说H3O+的杂化是Sp3.
杂化通常是原子轨道的混合形成一个新的杂化轨道。
我们也可以从VSEPR图中确定分子的杂化,我们将在下一部分讨论。
H3O+分子几何
H3O+的分子形状为三角金字塔,电子几何形状为四面体。
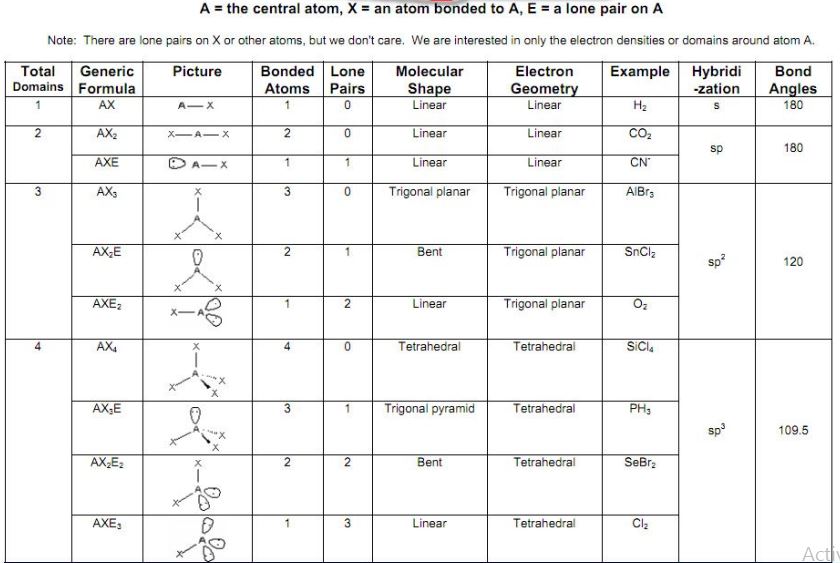
从上面的图表中,我们可以看到水合氢离子是AX3E型分子
(A=中心原子,X=成键原子,E= A上的孤对)。
因此根据VSEPR图,H3O+的分子形状为三角金字塔,电子几何形状为四面体。
下面的图片解释了上述所有的概念,

分子形状和电子几何之间有一个明显的区别。
在分子形状中,在确定分子结构时只考虑原子。
但是在电子几何中,所有的电子对都被考虑在内。
换句话说,孤对在电子几何的情况下被考虑,而不是在分子形状。
从VSEPR图,杂交也可以确定,如我前面所述。我们还可以看到水合氢离子有Sp3杂化。
形成极性的原因还在于H3O+分子中氧原子上存在孤对。
净偶极子是一个非零值,使H3O+成为极性分子。
H3O+分子轨道图
任何分子的分子轨道图都能告诉我们分子中轨道的混合情况。
说到H3O+的重叠图,它和H2O很相似,只是少了一个电子,多了一个氢。
下图为H3O+的分子轨道图,也为H2O的分子轨道图,供参考。
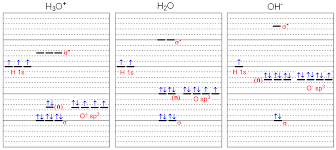
在上图中,左边解释了水合氢离子的MO图。
MO由3个氢原子的原子轨道组成。而且,O+原子轨道比水原子轨道少一个电子。
它们一起构成了分子的MO,在非成键轨道上有2个电子。
而且成键轨道上有6个电子反键轨道是空的。
图像中还包含了OH-的MO图,供参考。
从分子轨道图中,我们可以看到只有水合氢离子发生了sigma键,这表明在这个离子中只有正面重叠是可能的。
这是水合氢离子分子轨道图的解释。
MO图可以帮助我们找到化合物的成键顺序,从而给我们提供诸如键长、化合物的稳定性等信息。
结论
本文围绕水合氢离子的结构、成键和杂化展开。分子轨道图也作了解释。
水合氢离子有几种用途,我之前解释过。学习基础知识将有助于你更好地理解反应,并对水合氢离子有一个清晰的认识。在这之后,你可以很容易地理解所有与水合氢离子有关的东西。
我希望这篇文章在某种程度上对你有所帮助,希望你在最后能学到一些知识!
如果有任何疑问,欢迎问我,祝你阅读愉快!




