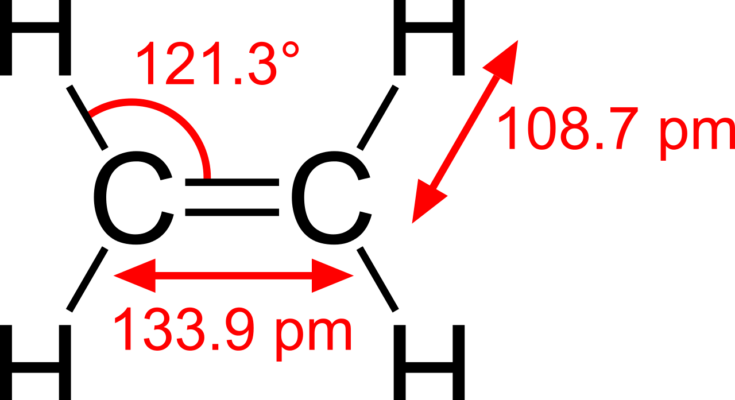
乙烯是一种碳氢化合物,化学式为C2H4。它是一种无色气体,带有麝香或微弱的气味。它是易燃的。很多人可能会怀疑乙烯是不是极性的。在这篇文章中,我将回答这个问题,并让您了解确定分子极性的参数。
那么,C2H4是极性还是非极性?乙烯(C2H4)由于其对称(线性)的几何形状,本质上是非极性的。另一个原因是由于几乎相同的电负性,碳氢键是非极性的。结果乙烯分子的偶极子为零。
乙烯是一种可燃气体。它的外观无色,有麝香味。IUPAC对乙烯的称呼是乙烯。
1901年,一位名叫迪米特里·内尔朱鲍的俄罗斯科学家首次发现了它。
它是烯烃家族中最简单的碳氢化合物。它被用于许多化学工业。它的主要产品是制造聚乙烯,也被称为塑料。
聚乙烯塑料是一种含有一系列乙烯分子的聚合物。
如果我们讨论乙烯分子的化学组成,它由2个碳原子和4个氢原子组成。
两个碳原子以双键共价连接。氢原子和碳原子之间通过一个共价键相连。
C2H4分子的分子质量为28.054 g·mol−1。可以计算如下
C2H4的摩尔质量= 2 * 12 (C的摩尔质量)+ 4 * 1 (H的摩尔质量)= 28.054 g·Mol−1。
分子相对于碳原子呈线性。通常线性分子在本质上是非极性的。
原子的电负性是它吸引成键电子对的强度。它是决定分子极性的一个重要因素。
碳的电负性是2.55,氢的电负性是2.2。C-H键是非极性的,因为两个原子的电负性几乎相同。

什么是极性分子和非极性分子?
分子受到原子间作用力的约束,包括金属键、氢键、离子键和共价键。
离子键和共价键是上述所有键力中最强的。
共价键是指原子共用电子以稳定原子的键。这些电子也被称为成键电子对。
键可以是单键(单电子对)、双键(两个电子对)和三键(三个电子对)。
极性分子电荷分布不均匀的分子称为极性分子。
这些分子具有非零偶极矩。偶极子是电荷和正负电荷中心之间距离的乘积。
如果两个原子的电负性不同,那么形成一个极性共价键的两个原子就是极性的。
很少有极性物质的例子是NF3, NCl3, H2O。你可以查看原因NF3极性.
非极性分子电荷均匀分布的分子称为非极性分子。
这些分子偶极矩为零。而且,一般认为非极性分子的形状是对称的。
形成非极性共价键的原子具有相等的电负性。此类化合物的例子有BeCl2, SF6。你可以查看原因无极性的BeCl2.
为什么C2H4是非极性分子?
乙烯由2个碳原子和4个氢原子组成。碳碳键是双共价键,即;发生了两电子对的共享。
碳的价电子是4,氢的价电子是1。两个碳原子彼此共用两个电子,两个电子来自两个与碳原子共价连接的氢原子。
结果,碳和氢都得到完整的八隅体,形成中性分子C2H4。
碳的电负性(2.55)和氢的电负性(2.2)也几乎相同,因为C-H键也是非极性的。
分子呈线性,即;对称的。因此,整个分子仍然是非极性分子。
C2H4分子是非极性分子,偶极矩为零。
影响分子极性的因素
电负性:原子的电负性是衡量原子吸引共用成键电子对向其一侧的强度。
具有较高电负性的原子将键合电子拉得更近,从而获得部分负电荷,而其他原子则获得部分正电荷。
如果构成一个分子的两个原子的电负性不同,那么这个分子本质上就是极性的。
结果,分子中产生了正极和负极。
分子的极性与原子的电负性之差成正比。
偶极矩:分子的偶极子是测量分子极性的数值。
分子的偶极子越大,其极性就越大。其SI单位为德拜,用D表示。
从技术上讲,它是原子上的电荷和正负电荷中心之间的距离的乘积。
D = q * r
几何形状:分子的形状是检验分子极性的一个重要参数。
通常观察到,对称形状的分子在本质上是非极性的,而非对称形状的分子是极性的。
请注意:如果非极性分子内部也存在极性键,则由于分子的对称形状,这些键的极性相互抵消。
下图是乙烯的几何分子结构
C2H4的性质
- 乙烯在室温下是一种无色气体,有麝香味。
- 它是易燃的。
- 该物质的熔点为−169.2°C或−272.6°F,沸点为−103.7°C或−154.7°F。
- 在15℃的温度下,该气体的密度为1.178 kg/m3。
- 在25°C的水中溶解度为0.131 mg/mL。
C2H4的用途
- 它主要用于制造塑料(聚乙烯)是由C2H4分子串联而成的聚合物。
- 它也用于不同化学反应中的卤化反应。
- 在美国和欧洲,90%的乙烯用于生产聚乙烯、二氯乙烯、环氧乙烷和乙苯。
- 乙烯被氧化形成环氧乙烷,环氧乙烷进一步用作制造洗涤剂和表面活性剂的原料。
结论
乙烯(C2H4)是一种线性分子,两个碳原子之间有双键(C=C)。碳氢键也是非极性的,因为它们的电负性几乎相同。
因此,整个分子是非极性的。
所以朋友们,如果你对C2H4的无极性有任何问题,你可以在评论区问他们。我们会尽快与您联系。