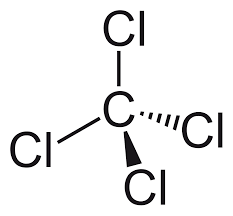
四氯化碳化学式为CCl4,是一种有机化合物。它是一种无色液体,有甜味。直接接触对人体也是有毒的。我们将详细研究CCl4的性质。学化学的学生可能会怀疑CCl4是极性的还是非极性的。因此,在这篇文章中,我将回答这个问题,并将涵盖周围的主题。
那么,CCl4是极性的还是非极性的?CCl4(四氯化碳)本质上是非极性的。虽然由于氯(3.16)和碳(2.55)的电负性不同,C-Cl的四个键是极性的,但CCl4是非极性的,因为CCl4分子的对称几何结构(四面体)使键的极性相互抵消。
四氯化碳是IUPAC对CCl4的称呼,它在室温下以液态存在。它会产生一种甜的气味,在较低的浓度下很容易被闻到。
1839年,亨利·维克多·雷纳德发现了它。
CCl4分子有1个碳原子连着4个氯原子。C-Cl的四个键都很相似,而且彼此对称。
重要的是要理解化合物的对称性是决定化合物极性的一个非常重要的因素。
这可以理解为碳原子和氯原子的电负性值不同,即C= 2.55, Cl= 3.16。使碳氯键成为极性共价键。
因此,所有四个碳-氯键都有一个偶极矩值。但是由于四个键的对称性,碳氯键的偶极矩被相反的碳氯键抵消了。结果,净偶极矩为零,使CCl4成为非极性分子。
甲烷气体(CH4)也有与CCl4相同的结构。
什么是极性分子和非极性分子?
值得注意的是,如果一个分子的净偶极矩为零,则该分子被认为是极性的。然而,在非极性分子中也可能存在极性键。
如前文在CCl4中所讨论的,C-CL具有一定的偶极矩值,具有极性,但整体CCl4分子具有非极性,因为CCl4分子的净偶极矩为零。
极性分子:这些分子的净偶极矩为正值。这些分子也具有不对称的几何结构。如果形成化学键的两个原子的电荷分布不均匀,那么化学键就是极性的。电子在两个原子之间不是均等地共享的。
在这种化学键中,电子对被轻微地推向两个原子中电负性更强的原子。由于电负性的不同和几何形状的不对称,这些分子变成极性的。
非极性分子:净偶极矩为零的分子为非极性分子。在这些分子中,几何结构也是对称的。
在形成化学键的两个原子中,如果电荷均匀地分布在两个原子上,这个化学键就被称为极性键,这意味着两个原子平均地共享电子。
为什么CCl4是非极性的?
由于CCl4具有对称的四面体几何结构,因此在本质上是非极性的。虽然C-CL键本质上是极性的,因为碳原子和氯原子的电负性不同。
因此,C-Cl键也有偶极矩。但由于其对称结构,净偶极矩相互抵消,形成了CCl4(四氯化碳)非极性分子。
分子的极性取决于下面讨论的各种因素。
影响化合物极性的因素
电负性在两个原子之间的化学键中,如果两个原子的电负性不同,则称该化学键为极性键。两个原子的电负性差越大,键的极性就越大。
但重要的是要知道分子内部有极性键也可以是非极性的,因为它的对称结构。在这种情况下,化学键的极性相互抵消。
几何结构具有对称几何形状的分子本质上是非极性的。对于对称分子,净偶极矩值为零。
偶极矩:具有净偶极矩的分子本质上是极性的,而具有零偶极矩的分子本质上是非极性的。
CCl4的几何结构
如果我们讨论四氯甲烷的几何结构,这四个化学键相对于其他的化学键方向是对称的。碳原子是由四个碳氯键连接的中心原子。
碳原子的最外层有4个电子,所有的4个键都参与了共价键的形成,碳原子上没有留下孤对。
CCl4形成了四面体几何结构,CCl4分子的键角约为109.5度。
四氯化碳与碳的一个s轨道和三个p轨道形成sp3杂化。
CCl4中所有的非成键电子都倾向于相互间产生排斥力,形成109.5度的键角,形成四面体形状。
关于价电子和路易斯结构的详细信息,你必须通过lewis结构,CCl4杂化.

CCl4的合成
四氯甲烷的形成是在1839年由法国化学家亨利·维克多·雷纳德完成的。它是由氯仿和氯反应合成的。
但是现在,合成四氯甲烷的过程是通过氯处理甲烷来完成的。反应如下所示
CH4(甲烷)+ 4Cl2(氯)—> CCl4 + 4 HCl(酸)
在20世纪50年代之前,制造四氯化碳的工艺是在105 ~ 130摄氏度的温度下用氯处理二硫化碳。
CS2(二硫化碳)+ 3Cl2(氯)—> CCl4 + S2Cl2
CCl4的物理化学性质
- CCl4(四氯化碳)在室温下以液体形式存在。
- 它是一种无色液体,也有甜味。
- 四氯化碳的熔点在零下23摄氏度左右。
- 它的沸点在76摄氏度左右。
- 四氯化碳的几何形状是对称的四面体。
- 四氯化碳的密度约为1.5867 g cm−3。
- CCl4可溶于氯仿、甲酸、醇、醚、CS2、石脑油、苯。
- CCl4在20℃时的蒸汽压为11.94 kPa。
- CCl4本质上是有毒的,它具有消耗臭氧的特性,也被归类为温室气体。
CCl4的用途
- 四氯甲烷由于其非极性性质,成为许多非极性物质的优良溶剂。
- 它是合成氯基有机化合物的良好氯源。
- 由于CCl4分子中没有氢原子,它在核磁共振波谱学中也有很大的用途。
- 四氯甲烷在灭火器中有很大的用途,它通过熄灭火焰来防止火灾。
结论
CCl4分子具有对称的四面体结构,本质上是非极性分子。然而C-Cl键是极性共价键,但四个键相互抵消极性,形成非极性CCl4分子。
因此,在这篇文章中,我试图涵盖四氯化碳分子(CCl4)的非极性性质。如果你们对此有任何问题,可以在下面的评论区提问。我们会尽快与您联系。