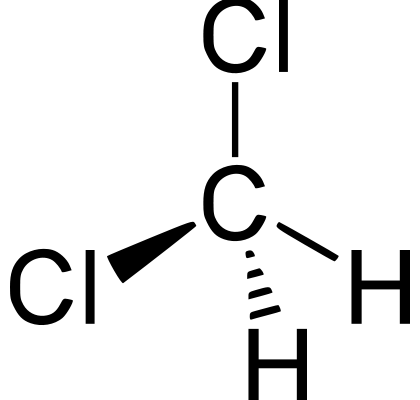
CH2Cl2通常被称为二氯甲烷或二氯甲烷,是一种透明、无色、易挥发的液体,具有微甜的气味。它是从火山和大型藻类中自然获得的。虽然与水不相溶,但用作许多有机反应的溶剂。许多学生对它是极性的还是非极性的有疑问。在本文中,我们将对其产生的根本原因进行研究。
那么,CH2Cl2是极性的还是非极性的?由于CH2Cl2具有四面体的几何形状以及碳、氢和氯原子的电负性差异,因此它是一种极性分子。这在C-Cl和C-H键之间形成了偶极矩,整个分子的净偶极矩为1.67 D。
甲基氯主要是由工业排放产生的。它是通过在400-500°C的高温下用氯处理甲烷而产生的。
以下是CH2Cl2生产过程中发生的化学反应。
CH4 + Cl2——热——> CH3Cl + HCl
CH3Cl + Cl2——热——> CH2Cl2 + HCl
什么是极性分子和非极性分子?
为了确定和区分分子的极性或非极性性质,在我们将要讨论的子主题中有以下几个关键点。
首先,让我们对极性分子和非极性分子有一个简单的概念。
极性分子:原子间共享的电子比例不等的分子。这表明原子的电负性不同。
电负性较高的原子将共享的键合电子稍微吸引到其一侧,从而获得部分负电荷,而其他原子则获得部分正电荷。
这种电负性的差异在键上产生了一个净偶极矩,使键具有极性。
如果我们谈论分子几何,通常可以看到极性分子的形状是对称的或扭曲的。
很少有极性分子的例子是HBr, SO2等。你可以查看原因HBr极性。
根据大多数著名的书籍,在极性分子中,原子间的电负性差是0.5到1.6。如果电负性差小于0.5或大于1.6,化学键就是非极性的。
如果两个原子的电负性不同,电负性高的原子会把共用的成键电子拉到它的一边。
因此,电负性越强的原子周围的电子密度越高,而其他原子的电子密度越低。
极性程度因元素而异,有些元素具有极低极性,而有些元素具有很强的极性
非极性分子:原子间共用相等比例的成键电子的分子是非极性分子。
这样的原子中没有相反的极点。这种分子的形状是对称的。
有可能一个非极性分子内部有极性键,但由于对称的形状,这些极性键的偶极子相互抵消。
它的意思是,当原子之间的电荷相互抵消,原子之间的极性键排列方式相同时,就形成了非极性分子。
非极性分子的例子有XeF2、CO2等。你可以查看原因XeF2无极性。
所有惰性气体和同核双原子分子都是非极性的。
为了确定化合物的极性和非极性,建议修改基本的化学术语,如电负性,偶极矩,几何和分子的形状,这将更清楚。
化学重要术语
电负性:电负性描述了原子将电子对吸引到其一侧的强度。
这为分子中原子的电子构型提供了一个更清晰的概念。
一个原子对电子的影响越强,它的电负性值就越大。
极性键中的电子被移到电负性更强的原子附近。
结果,电负性较高的原子获得部分负电荷。电负性差越大,分子内的电子分布越极化。
根据元素周期表,元素的电负性从左到右递增,在一组内依次递减。
因此,出现在右边的元素往往具有最高的电负性,所以卤素族元素的电负性最大。
金属是电负性较小的元素,第1族金属的电负性最低。
偶极矩测量分子中两个原子间化学键极性的第二个重要因素是偶极矩。
它测量系统中负电荷和正电荷的分离。
在数学上,分子的偶极矩也可以被称为原子上电荷的大小和它们中心之间的距离的乘积。
分子的形状:另一个决定极性的因素是分子的形状。复杂分子的极性或无极性取决于正负电荷重叠的整体中心。
如果一个分子是完全对称的,那么每个分子上的偶极矩就会抵消,使分子是非极性的。
如果一个分子的结构不对称,就称其为极性分子。
检查化合物极性的关键点
- 极性的强弱是通过比较原子成键的电负性来确定的。
- 极性可以通过分子的形状和几何形状来测量。
- 偶极矩在决定化合物的极性方面也起着重要作用。
为什么CH2Cl2是极性分子?
- C-Cl键比C-H键更具极性。
- 由于氢原子的电负性比氯原子低,电子从氢原子向氯原子的拉力导致电荷的不均匀分布。
- 氯有吸引电子的能力,使二氯甲烷的一边部分带正电,另一边带负电。
- 化学键的极性是通过比较成键原子的电负性来确定的。
- 在二氯甲烷的情况下,所有键原子的电负性如下
氢=2.2,碳=2.5,氯=3.1。 - 所以C-H=0.3和C-Cl=0.6的电负性差。这证明了CH2Cl2是极性的,但是中等极性的,因为它们的电负性相差很小。
- CH2Cl2分子的价电子总数是20。碳有4个价电子氢有1个电子氯有7个价电子。
- 所以一共有20个价电子4*1+1*2+7*2=20
- 中心的两个碳原子分别和两个氢原子成键,和两个氯原子成键。20个价电子中,有8个参与成键。
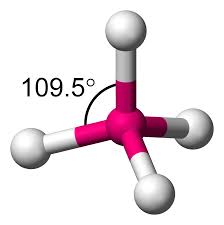
- 二氯甲烷中形成的键是共价的,因为中心碳原子杂化形成了所有的四个键。碳原子的杂化是sp3。
- CH2Cl2的分子排列方式是这样的,碳原子位于sp3杂化的中心。CH2Cl2的几何结构为四面体,化合物的形状为三角锥体。
二氯甲烷的应用
- 由于挥发性,它被用作一种溶剂,从各种表面和浴缸抛光去除油漆或清漆涂层。
- 在气雾剂工业中,它被用于喷涂油漆和杀虫剂。
- 最重要的是在食品工业中用于咖啡豆和茶叶的脱咖啡因。
- 它被用于食品和饮料行业的香料和其他调味料的加工。
- 在制药领域,它被用作溶剂。
- CH2Cl2被用来从植物中提取化学物质来制造类固醇、维生素和抗生素。
- CH2Cl2用于清洁医疗设备,不会引起腐蚀和加热损坏。
- CH2Cl2用作油墨稀释剂。
- 二氯甲烷用于金属表面、飞机部件、铁路轨道和设备的脱脂。
- 用于汽车产品的垫圈拆卸和为新垫圈准备金属零件。
- 在汽车工业中,CH2Cl2的蒸汽有助于去除汽车晶体管部件上的油脂。
- 二氯甲烷用于合成纤维和摄影胶片的制造。
CH2Cl2的副作用
- 它不可燃,但在高温下,它会释放出有毒的光气烟雾。
- 使用时要小心,因为它是剧毒的。
- 它会刺激眼睛、喉咙和鼻子。
- 它会扰乱神经系统。
操作CH2Cl2的注意事项
- 穿围裙和全袖防护服。
- 穿合适的鞋子覆盖整个脚。
- 始终穿戴个人防护装备、护目镜和安全手套。
- 在通风良好的地方工作。
- 由于它是高度挥发性的,所以应储存在一个凉爽,干燥的地方,在密封和标记的容器。
- 并且需要远离金属,光线和任何热源或火源。
结论
简而言之,我们发现CH2Cl2是极性的,原因如下:-
- 它的形状呈三角锥体。
- 这个化合物的几何结构是四面体。
- 碳-氢和碳-氯之间的偶极矩不抵消。
- C-H和C-Cl的电负性分别为0.4和0.6。
过度接触它会导致癌症、咳嗽、喘息、呼吸短促和吸入可导致头痛、精神错乱、恶心、呕吐、头晕和疲劳。