盐酸被称为盐酸或盐酸。它是卤化氢(HX)的成员之一。卤化氢是无机双原子分子,由于其倾向于在溶液中失去质子,因此充当阿伦尼乌斯酸。X是卤素家族(第17族)的一员,因此,它可以是氟、氯、溴和碘。
盐酸是氯化氢在水中的无色透明溶液。它是一种带有刺激性气味的强酸。
氯化氢溶液的熔点和沸点不是固定的,因为它们取决于其水溶液的浓度。同样,氯化氢溶液的pH值和密度也不是固定的。
如果我们打开一瓶浓缩的盐酸溶液,我们可以观察到空气中有刺鼻的气味。
盐酸存在于我们的胃中,有助于食物的消化。这种酸在胃里的高浓度会导致胃酸问题。
盐酸用于各种有机和无机化合物的合成,也用于离子交换的再生,用于水的净化。
那么,盐酸是离子的还是共价的呢?盐酸是一种共价化合物,因为氢和氯的电负性差小于2.0。然而,它不是一个真正的共价化合物,因为氯的电负性比氢强,因此,它会吸引一对共用的电子。因此,HCl分子是一种具有17%离子特性的共价化合物。
在HCl分子中,H-Cl键将作为偶极子,分别在氢原子和氯原子上带部分正电荷和部分负电荷。
盐酸中的部分电荷值为±0。027 × 10−18 C.
让我们详细讨论一下氯化氢的共价性质。
为此,我们需要从化学键的基本知识开始,即什么是化学键以及它是如何形成的。
化学键
首先,让我们来看看现代元素周期表。
我们都知道,现代元素周期表中的原子除了第18族成员之外,在自然界中是不自由存在的。因此,它们要么与同一个原子结合,要么与不同的原子结合,分别形成元素和化合物。
两个相同或不同原子之间的吸引力,有助于将它们结合在一起,这被称为化学键。
化学键是如何形成的?
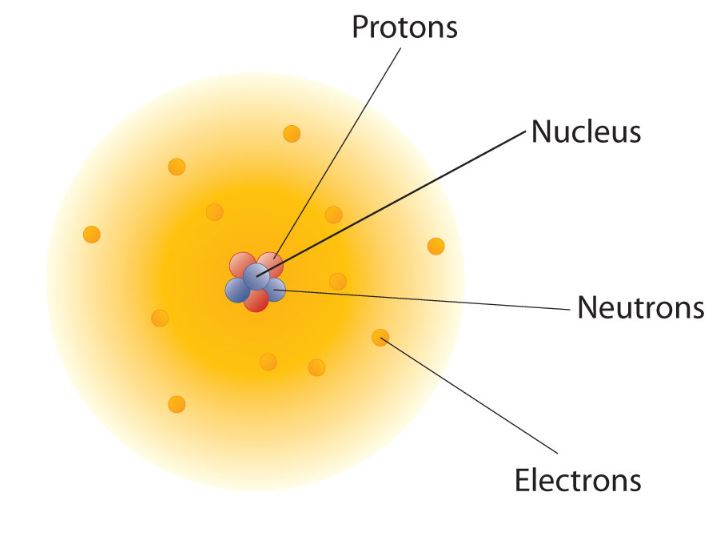
原子由亚原子粒子组成,即质子、电子和中子。在这三种粒子中,只有电子参与成键。
我们知道,原子的原子序数与原子中的电子数相对应。
现在,一个问题出现了,是否原子中所有的电子都参与成键?
不,不是所有的电子都参与成键。唯一存在于原子最外层的电子有助于键的形成。这些电子被称为价电子。
存在于原子内壳层的电子被称为核心电子,它们不参与键的形成。
因此,当两个原子之间共享电子密度时,化学键就形成了。原子间电子密度的共享可能相等,也可能不相等。
化学键的类型
分子中存在两种类型的化学键,即离子键和共价键。
离子键离子键是通过将电子从一个原子转移到另一个原子而形成的。在离子键中,正离子和阴离子之间有静电吸引力。
共价键共价键是由两个原子共用一对电子而形成的。共价键进一步分为单键、双键和三键,这取决于两个原子中共享的电子对的数量。
那么,如何区分一个化学键是离子键还是共价键呢?
显然,我们不能通过观察参与成键的原子来回答这个问题。我们需要一个定量参数来区分离子键和共价键。这个参数是电负性值。
让我们知道,什么是电负性?
电负性
它是原子吸引共用电子对的特性。原子的电负性值取自鲍林尺度。
如果化学键中两个原子的电负性差大于2.0,则该化学键被认为是离子键。然而,如果这个差值在鲍林尺度上小于2.0,那么就存在共价键。
为什么盐酸在自然界中是共价的?
以氯化氢为例,
氢原子的电负性值为2.20
氯原子的电负性值为3.16
H-Cl键的电负性差= 0.96
在鲍林尺度上,H-Cl键的电负性差仅为0.96,表明H-Cl键具有共价性质。
因此,氯化氢是一种共价化合物。
然而,氯化氢并不是一种真正的共价化合物。为什么是这样,什么是真正的共价化合物?
为什么盐酸不是真正的共价化合物?
真正的共价键是当分子中每个原子的电子都相等时形成的,如同核分子,即H-H, F-F和Cl-Cl等。
然而,当异核分子存在时,共价的性质或者我们可以说共价的纯度降低了。例如H-Cl, H-Br和H-I。在异核分子中,由于电负性值的不同,原子不平等地共享电子。
因此,HCl不是真正的共价化合物,因为氯原子的电负性(3.16)比氢原子的电负性(2.20)高,因此氯原子会吸引一对共用电子。

或者我们可以说氯化氢化合物中的H-Cl键是极性共价键。这意味着H-Cl键作为偶极子氢原子上带部分正电荷氯原子上带部分负电荷。
如果我们能计算出原子的部分电荷,那就很有趣了。那么,让我们计算一下氯化氢中氢原子和氯原子的部分电荷。
电荷被定义为分子偶极矩(µ)与极性共价键中两个原子之间的距离(d)的比值。电荷的测量公式如下:
Q = μ/d
偶极矩的测量单位是D(德拜),距离的单位是m,因此电荷的测量单位是D/m或C(库仑)。
氯化氢偶极矩为1.05 D,氯化氢中氢与氯原子的距离为127.4 * 10-12 m。
1 D = 3.33 × 10−30 C. m
如果我们把上面方程中的值代入,氢原子上的部分电荷是0.027 x 10-18 C。
氯原子上有相等相反的电荷,即- 0.027 x 10-18 C。因此,氯化氢化合物的部分电荷为±0。027 × 10−18 C。
我们的下一步是估计氯化氢中从氢原子转移到氯原子的电子的百分比,这是共价键中已知的离子特性。
我们知道一个电子的电荷是1。6022 × 10−19 c。
离子特性百分比=(原子的部分电荷∗100)/单个电子的电荷
=(0。027 × 10−18 * 100)/1。6022 × 10−19 c
= 17 %
因此,在氯化氢中,只有17%的电子密度从氢原子转移到氯原子。
这证实了氯化氢中的H-Cl键是极性共价键,而不是离子键。这是区分离子键和共价键的另一个标准。
因此,氯化氢分子是一种具有17%离子特性的共价化合物。
结论
在这篇文章中,我们研究了氯化氢化合物的共价性质。
简而言之,氯化氢是一种共价化合物,基于两个HCl分子原子间的电负性差异。然而,这种共价化合物具有一些离子性质,计算为17%。它证实了HCl分子中H-Cl键作为极性共价键的性质。
综上所述,氯化氢分子是具有±0.027 x 10−18 C部分电荷的极性共价化合物,离子性质为17%。




