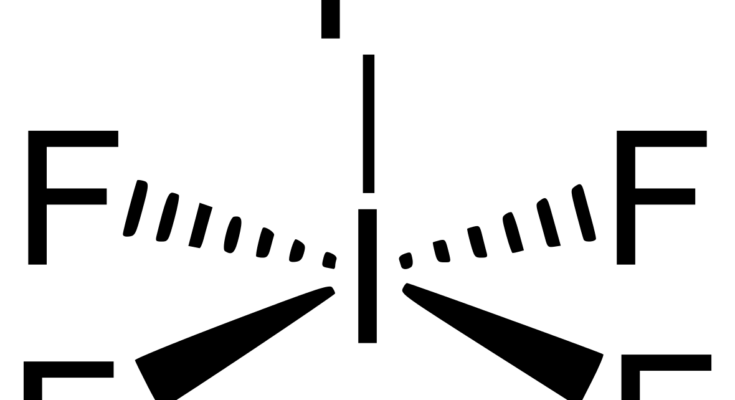
五氟化碘的化学式为IF5,是一种卤素间化合物。它是一种无色液体,由亨利·莫桑于1891年发现。
许多反应发生在几种化合物与五氟化碘混合的过程中。许多理科生可能会对IF5是否极性有疑问。我将回答这个问题,也将讨论周围的主题。
那么,IF5是极性还是非极性?IF5本质上是极性的。根据VSEPR理论,由于孤对和键对斥力的存在,分子具有弯曲的几何结构,因此分子中电荷分布不平衡。氟的电负性比碘强,这是因为偶极矩的产生使IF5成为极性分子。
IF5的IUPAC首选名称为氟化碘(V)。它被归类为一种卤素间化合物。它是一种无色液体的外观。虽然不纯的IF5呈黄色。
在许多化学反应中,它作为氟化试剂有许多用途。
五氟化碘最初是在氟气体存在下燃烧碘而制备的。它本质上是有毒的,也是一种氧化剂。
如果我们讨论五氟化碘的化学组成,这个分子由五个氟原子和一个碘原子组成。
碘的最外层有7个价电子氟的最外层也有7个价电子。
两个原子都需要一个电子才能稳定。在IF5中,这五个电子通过共享碘原子的一个电子得到稳定碘原子缺少两个电子可以共享它们以孤对的形式存在于碘原子上。
它是由固体碘在氟气体中燃烧形成的。同样的方法用于在更好的反应环境下生产IF5。
I2(固体碘)+ 5F2(氟气体)——> 2IF5
什么是极性分子和非极性分子?
极性分子如由共价键连接的分子中的两个原子,如果成键的电子对不是相等地由两个原子共享,则称为极性原子。
这意味着这类分子中两个原子的电荷分布是不一样的。这类化合物的例子有IF5, CO。
在这些分子中,原子的电负性存在差异。电负性越强的原子吸引成键电子对的影响越大,从而获得部分负电荷。
结果,在分子IF5中发生了不平等的电子共享。
这些分子的偶极矩也是非零的。
你可以查看原因丙酮极性.
非极性分子如分子的原子以相等的比例共用成键的电子,则称为非极性分子。在这样的分子中,两个原子的成键电子分布相等。
因此,两个原子的电子密度相等。这类化合物的例子有O2, CO2。
在这些电子中,几何形状是对称的。这是因为净偶极矩也是零。
看看原因无极性的BeCl2.
为什么IF5是极性分子?
一个碘原子和五个氟原子结合形成一个IF5分子。一个孤对留在碘原子上,五个氟原子与碘原子形成共价键。
根据VSEPR理论,孤对和键对相互排斥。类似地,在IF5的情况下,孤电子对和键对面临一个排斥力,导致键角彼此设置为大约90度。
碘上的孤对位于五氟化碘分子几何的轴向位置。
氟的电负性比碘的电负性大,这是由于两个原子上的电荷分布不相等。这意味着在I-F键中,电子对不是被两个原子平均占有的。
因此,I-F键的偶极矩值是非零的。
所有I-F键的偶极矩的方向是相同的,因此,净偶极矩增加并导致一个非零值,决定了IF5分子的极性。
有一些因素会影响分子的极性。下面将详细讨论这些问题
影响化合物极性的因素
电负性一个分子的原子的电负性是衡量它能有多强地吸引成键的电子。
如果两个原子的电负性不同,那么形成共价键的两个原子就是极性的。
形成共价键的两个原子的电负性差异越大,极性也就越大。
偶极矩它是化合物极性的量度。偶极矩的值越大,化合物的极性就越大。
因此,化合物的极性与其偶极矩成正比。
在数学上,偶极矩是用原子上的电荷和原子间距离的乘积来计算的。
Q =原子的电荷
键长
D =偶极矩
D = q * r
分子几何分子的几何形状在检查分子的极性方面起着重要的作用。通过观察分子的几何结构来确定分子的极性是很容易的。
如果分子具有对称结构,则分子本质上是非极性的。如果形状不对称,分子就是极性分子。
IF5的分子几何结构

IF5有5个氟原子与碘原子共价键,在碘原子上留下一个孤对。
根据VSEPR理论,孤对和键对相互排斥,导致分子形状的扭曲。
同样,I_F键上碘原子和键对上的孤对产生排斥力,键角设置为键间夹角约为90度。
结果,形成的IF5分子的形状为方形锥体。
四个I-F键在一个平面上形成一个正方形,一个I-F键在与孤对相反的轴上,也轴向分子的方向。
上图是五氟化碘分子的几何结构。有关更多详细信息,您也可以参考IF5的lewis结构.
IF5的性质
- 五氟化碘在室温下是无色液体。
- 该分子的密度约为3.250 g/cm3。
- IF5的熔点为9.43°C或48.97°F。
- 它的沸点约为97.85°C或208.13°F。
- 它很容易与水反应生成HF酸(氢氟酸和碘酸)。
- 液态五氟化碘的粘度为2.111 mPa·s。
IF5的用途
- 氟化碘主要用于制造含氟的烷基碘化物。
- 碘也被用来生产制造聚合物的中间化合物。
- IF5在有机合成中作为氟化剂有很大用途。
结论
由于碘原子上存在孤对,IF5分子呈方形五角形分子结构。氟的电负性比碘强,因此I-F键的极性上升。
所有的I-F键导致完整的IF5分子的净偶极矩,使其成为极性化合物。