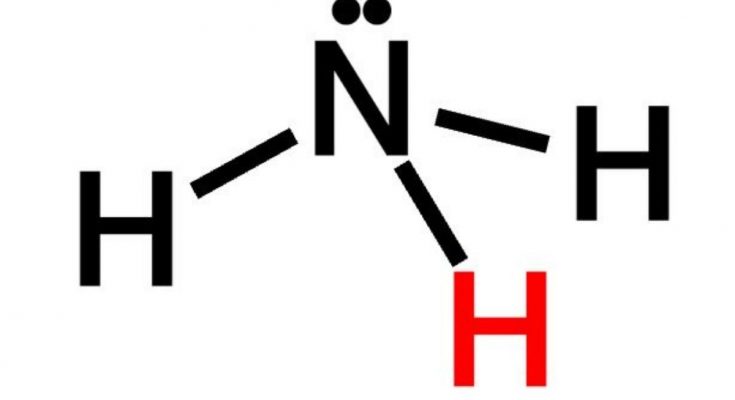
你知道鱼粪便中最多的成分是什么吗?氨!是的,你没看错。
氨(NH3)由氮和氢组成,化学式为NH3。它是无色气体。它有一种特别刺鼻的气味。少量存在于空气和土壤中。它是由含氮有机物如尿素的衰变形成的。
通常存在于湖泊和溪流等水体中的植物和藻类中。微量的它对人体是有毒的。
氨被称为二元化合物,这意味着它是由两种不同类型的原子形成的。
它也是最简单的二元氢氮。NH3在标准压力下在−33.34°C(−28.012°F)沸腾。它必须在压力下或低温下储存。
让我们在这篇文章中探究氨是共价化合物还是离子化合物!
那么,NH3是离子还是共价?氨是一种共价化合物,因为氢和氮原子之间的电负性不同,即;0.9.氮原子和氢原子彼此共用电子,形成一个共价键,从而形成共价NH3化合物。
非金属如氮和氢原子结合时处于自然状态。
化合物没有任何接受或提供电子的倾向,也没有共用价电子的倾向。因此,它使氨成为共价化合物。

氨为什么是共价化合物?
氨是共价的,因为氮和氢的电负性不同。氮的原子序数是7,而氢的原子序数是1。
如果我们分别深入研究氮和氢的电子排布,我们会发现氮的第一能层有两个电子,第二能层有5个电子。
氢原子在第一能层总共只有一个电子。如果氮必须变成惰性的那么它必须在第二层电子层多出3个电子。
要稳定一个氮原子,总共需要三个氢。而三个氢都需要一个电子才能稳定。
通过这个计算,我们可以看到氮确实有空间容纳三个电子,而且它可以很容易地与三个氢原子共享电子。
因此,三个氢原子将与一个氮原子反应,相互分享电子,并变得完全惰性。
这种反应使化合物具有共价。
我们也可以应用法扬法则来证明氨的共价性质。在NH3中,正离子是氢离子(H+),负离子是氮(N-)。
阴离子(-ve离子)明显大于正离子(+ve离子)。这意味着氨化合物的共价性质是由于法扬规则。

什么是共价化合物?
共价化合物-两种非金属元素共用电子形成稳定化合物。这些化合物共用相同数量的电子而变成惰性的。存在于这种化合物中的键称为共价键。
这些债券可以分为三类:
1.单共价键
2.双价共价键
3.三重共价
单个共价键确实只与另一个原子共用一个电子。氨是表现单共价键的最好例子。
双价键与另一个原子共用两个电子来完成价电子。例如:大气中的氧气(O2)。
三共价键是指两个原子之间共用三个或三个以上的电子,形成惰性化合物。例子:N2。
您可以参考氧中的共价键.
形成共价化合物的条件
1.两个原子都应该有很高的电离势
2.两个原子都应该有很高的电子亲和度
3.电负性差应该为零或可以忽略不计
极性和非极性共价化合物
当共享的电子对在两个原子之间的距离不相等时,共价化合物被称为极性化合物。
这种情况发生在一个原子的电负性高于另一个原子时,它倾向于把电负性较低的电子拉到自己的一侧。
这种情况会在电负性较高的原子上产生轻微的负电荷,而在另一个原子上产生轻微的正电荷。在这种情况下,化合物被称为极性共价化合物。
比如氟化氢,氨,水。
当共用电子对在两个原子之间的距离相等时,共价化合物被称为非极性化合物。当两个原子的电负性相等时就会发生这种情况。
这些共价化合物平等地共享它们的电子,被称为非极性共价化合物。比如H2 O2 N3。
查看这篇文章H2极性.
共价化合物的性质
1.在标准室温和常压下,它们可以以固体、液体或气体的形式存在。
2.低熔点和沸点
3.溶于有机液体,不溶于水
4.导电不良
什么是离子化合物?
离子化合物是金属元素与非金属元素反应形成的。金属提供电子,非金属接受电子。
离子化合物和电价化合物是一样的。例如:NaCl, MgCl2。
离子化合物的性质
1.这些是固体,坚硬但易碎。
2.熔融状态下的导电良导体
3.高熔点和沸点
4.溶于水,不溶于有机溶剂

氨的性质
化学性质
1.氨分解成它的主要元素,即;加热后的氮和氢。
2.水和氨反应生成氢氧化铵。
3.氨与酸反应时会形成相应的盐。
4.氨在空气中不燃烧,也不支持燃烧。
5.氨生成水和一氧化氮,最后在催化氧化过程中生成二氧化氮。
6.氨与盐酸反应时产生浓密的白色烟雾。
物理性质
1.它是无色气体。
2.它有刺鼻的气味。
3.它的蒸汽密度为8.5,比空气的密度要轻。因此,采用向下置换技术从空气中收集氨。
4.它本质上是基本的。
5.极易溶于水。
6.把红色石蕊变成蓝色。
氨的结构
VSEPR理论预测氨的形状为三角形金字塔。实验确定的键角为106.7°。
中心的氮原子有5个外层价电子,从每个氢原子那里得到一个额外的电子,总共有8个电子。
这八个电子形成三个电子对,呈四面体排列。
氨分子在室温下会翻转过来。一个相关的类比是一把雨伞在强风中翻了出来。

氨的用途
1.它被用作制冷剂冷却剂,因为它蒸发迅速,产生冷却。这些被称为氟氯化碳。
2.炸药生产需要氨。
3.氨可用作清洁剂。
4.它是肥料的主要成分。
结论
氨是一种共价分子,因为它有很强的电子分布。它由氢和氮组成。每个氢原子缺少一个电子,像氦原子一样变成惰性原子。氮少了3个电子才能有一个完整的外层。所以每个氢原子都和氮原子的三个外层电子共用电子。
氨中的氮是中心原子,而氢原子是附着在中心原子上的原子。在氮原子中,有三个价电子在氢原子中,有一个价电子。
氨分子(nh3)是由强N-H单键结合在一起的,这种单键是由一个氢原子和一个氮原子共用一个电子形成的。因此,所有四个原子实际上都有完整的外壳。