铵离子是氨(NH)质子化的结果而形成的多原子离子3.).它是一个带正电荷的离子,用化学式NH表示4+.
它是一种无机离子,通常作为不同动物代谢系统的废物形成。它被用于生产化肥、炸药等。土壤中铵离子的过量存在会引起酸化。
在本文中,我们将更多地了解NH4+以及它的不同性质。
让我们开始吧……
是北半球4+一个酸吗?
是的,NH4+是酸。它的pH值约为5.5,还能在水溶液中提供一个质子。NH4+离子在水溶液中不完全解离,因此NH4+被认为是弱酸。NH4+是碱氨(NH3)的共轭酸。化学方程如下:
NH4++ H2O——> h2O + nh3.+ H+
根据上面的方程,在水溶液中,铵离子随着质子的释放形成氨和水。
是NH4+一个碱性?
碱或碱是接受一个质子或提供一个电子的物质。它们的pH值在7以上,呈红色石蕊蓝。由于这些都不是铵离子的情况,它不能被认为是碱。
此外,与其他碱不同,铵离子不能产生OH- - - - - -水溶液中的离子,也不能将孤电子对提供给其他原子或分子。
因此,铵根离子+不是碱。
NH4 pH+
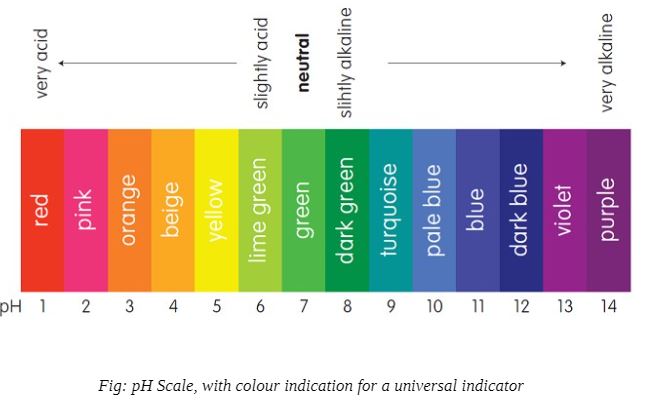
物质的pH值提供了其酸度或碱性的衡量标准。pH值高于7表示该物质为碱性物质,pH值低于7表示该物质为酸性物质,pH值等于7表示该物质为中性物质。
以铵离子为例,上述质子化反应也可以写成:
NH4++ H2O——> nh4Oh + h+
上述反应的平衡常数方程可以写成:
Ka = [NH4OH] [H .+[nh4 +]
现在,让我们试着找出0.1 M溶液中铵离子的pH值。
铵离子的Ka值为5.55 X 10-10.
而且,我们知道溶液中铵离子的初始浓度是0.1。
现在,假设有x摩尔的NH4OH和H+就形成了,让我们把这些值代入上面的反应。因此,
5.55 x 10-10= [x]/[0.1 - x]
由于Ka的值很小,我们可以考虑0.1 - x≈0.1
因此,x2 = 55.5 × 10-12
在此基础上,计算上述反应的x值,
得到x = 7.44 x 10-6
因此,[H+] = 7.44 X 10-6
现在pH = -log [H+]
= -log 7.44 X 10-6
= 5.13
铵离子溶液pH值低于7,属酸性。
此外,由于pH接近7,Ka的值小于1,这意味着NH4+呈微酸性。
为什么是NH4+酸性?
已经有相当多的理论来区分酸和碱。然而,有三个最重要的理论构成了酸碱化学的基础。它们是:
•Bronsted-Lowry理论:这个理论指出,酸是一种在水溶液中很容易提供质子的物质。质子被提取的难易程度提供了酸强度的衡量标准。

•阿伦尼乌斯理论:这个理论强调酸能够在水溶液中产生氢离子。
•刘易斯理论:这一理论将酸描述为一种物质,它很容易接受任何其他分子提供的孤电子对。
现在,考虑到以上所有的理论,让我们来看看铵离子。
如上所述,铵离子在水溶液中释放质子。因此,根据Bronsted-Lowry理论,它是酸的。
此外,铵离子在水溶液中解离形成氢原子和氨分子。因此,它也符合阿伦尼乌斯理论提出的酸的标准。
最后,看看刘易斯的概念,铵离子在它的中心原子上没有任何孤对电子,因此,它有接受其他分子提供的质子的倾向。因此,铵离子可以被正确地归类为路易斯酸。
是NH4+强酸还是弱酸?
为了理解这一点,让我们先描述一下什么是强酸或弱酸。
强酸是那些在水溶液中容易完全电离的酸。它们倾向于轻易地提供质子。
通常,它们的pH值远低于7,尽管它也取决于溶液中酸的浓度。强酸的例子有HCl, H2所以4, HBr等。
另一方面,弱酸是那些在水溶液中只部分解离的酸。它们也提供质子,但不像强酸那么容易。弱酸的例子有HCN, CH3.羧基,H3.阿宝4等。
看看H3PO4是酸还是碱.
现在,让我们来看看铵离子。
铵离子在水溶液中不能完全解离。这也从极低的酸解离常数(Ka)值可见。
NH的另一个原因4+NH是弱酸3.它是作为这个离子的共轭碱形成的,是一个弱碱,因此,很容易与水反应形成NH4+离子。
因此,大多数时候NH4+离子在溶液中保持结合。因此,铵离子是弱酸。
在这里,我们还必须理解酸解离常数的概念,它可以表示为:
•对于强酸,Ka >
•对于弱酸,Ka < 1
如前所述,NH的酸解离常数的值4+离子总是小于1。这进一步证实了铵离子的弱酸作用。
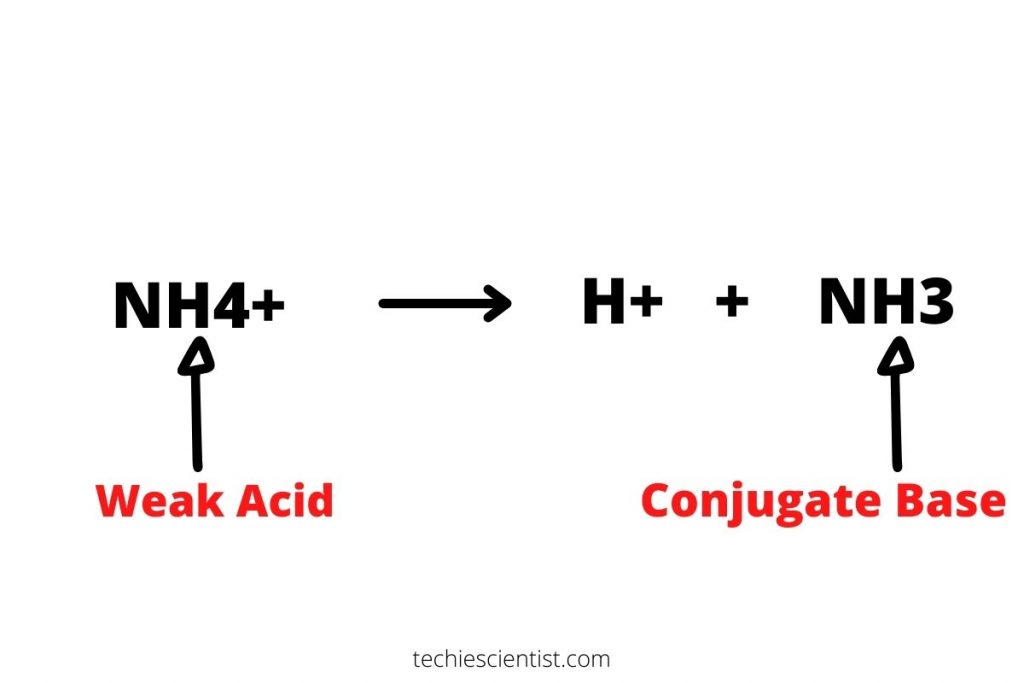
哪个是强酸NH4+或氨吗?
铵离子,即NH4+氨,即NH3.以共轭酸碱对的形式相互联系。铵离子在水溶液中失去一个质子形成氨。
我们已经知道酸的共轭碱是在酸给出它的质子时形成的,因此是NH4+作为质子酸而NH3.作为它的共轭碱。
反应可以写成:
NH4+(aq)—> NH3 + H2O
因此,NH4+离子作为酸肯定比NH强3.分子。
NH4和NH3哪个更稳定?
确定化合物稳定性的基本规则是中性分子总是比它们的离子更稳定。
在这个例子中,我们有氨,它是中性分子,另一方面,我们有铵离子,带一个正电荷。由此可见,NH3.会比NH更稳定吗4+因为后者被控告了。
然而,这里还要提到的一点是,在酸性条件下,自然界中酸性的铵离子变得相对稳定,而氨分子往往不那么稳定。
同样,由于氨的pH值接近天平的碱性一侧,它在碱性环境中会更稳定。
NH4是缓冲物吗?
在化学中,含有几乎相等浓度的酸和碱的溶液被称为缓冲液。
这些是用来保护溶液的pH值不因添加少量的酸或碱而发生任何变化。
通常,它们是滴定反应的结果。每个缓冲溶液都有一个pH值范围,这是有帮助的,即如果溶液的pH值改变超过了这个范围,添加的缓冲溶液可能无助于调节溶液的pH值。
为了有效地稳定溶液的pH值,缓冲溶液理想地由弱酸及其共轭碱制成。在铵离子的情况下,含有最佳混合的NH4+和NH3的溶液作为有效的缓冲溶液。
属性和用途
•铵离子的分子量为18.039 gm。
•它是一种无机化合物,以离子的形式存在。
•NH的几何形状4+离子是四面体。
•它是一种氮氢化物,表现为单质子酸。
•是氨的共轭酸。
•正常情况下,NH4+离子表现为汞合金,而在高压下则表现为金属。
相关的话题
结论
铵离子表现为弱酸,pH值约为5.5。
铵离子通过给出一个质子而表现为Bronsted酸,通过提供氢离子表现为Arrhenius酸,通过接受一对孤电子表现为Lewis酸。
铵离子在水溶液中释放一个质子形成氨,氨分子在水溶液中接受一个质子形成铵离子,铵离子与氨分子是共轭酸碱对关系。
铵离子是弱酸,因为它们在水溶液中不能完全解离。此外,它的Ka值小于1,这是弱酸的特征。
铵离子在酸性环境中更稳定,而它们的共轭碱氨在碱性环境中更稳定。
具有最佳氨和铵离子浓度的溶液充当缓冲液,可用于调节溶液的pH值。
阅读快乐! !