一个经常被问到的问题是二氧化硫是离子键还是共价键。在回答这个问题之前,了解二氧化硫的某些特性是很重要的。它是一种有毒无色气体,间接导致温室气体。
尽管二氧化硫在地球大气中的含量并不丰富,但其存在的痕迹可造成严重的健康影响。这种无色气体带有刺激性气味,可导致窒息或窒息。二氧化硫被广泛用于制造化学品、制浆造纸、加工食品和金属。
现在迫在眉睫的问题是,二氧化硫是离子还是共价?二氧化硫是一种共价化合物,因为在二氧化硫的情况下,两个具有相似电负性的原子试图结合在一起。在此过程中,两个原子之间电负性的微小差异导致共享电子键形成共价键。
在原子共享电子以完成八隅体结构的情况下,这导致形成共价键合化合物。
为了了解二氧化硫的共价键,有必要讨论二氧化硫的刘易斯结构、VSEPR理论以及二氧化硫的酸性或碱性。
路易斯结构将给出一个清晰的概念,共振结构导致形成共价键的二氧化硫。
VSEPR理论有助于确定影响SO2共价键的分子二氧化硫的极性。
由于SO2分子形成共价键,SO2的Sigma键和Pi键会产生重要影响。
硫和氧在元素周期表中的位置
在元素周期表中,硫属于VI A族。硫是VI A族的第二个元素,属于第三个周期。
硫有三层,分别是K, L和M。
与硫相似,氧也属于VI a族。氧是该族的第一个元素,因此属于第二周期。它有两层,即K和L。
| 硫 | 氧气 | |
| 集团 | 第六个 | 第六个 |
| 元素在组中的位置 | 第二个 | 第一个 |
| 期 | 第三期 | 二期 |
| 壳数 | 3 - k, l和m | 2 - k, l |
| 电子总数 | 16 | 8 |
| 价电子数 | 6 | 6 |
路易斯结构
通常被称为电子点结构或刘易斯点结构,是在图表的帮助下,在分子元素之间形成的键的表示。
你还必须把写在上面的文章读出来lewis结构,SO2的几何结构.
结构的图解表示表明,分子的所有元素形式电荷为0。

共振的第一结构
硫的电负性为2.58,氧的电负性为3.44。因此,本质上电负性更强的氧将被放在两边。
具有6个价电子的非金属元素将形成共价键。
硫可以和其中一个氧原子形成双价键。
结果是两个原子都有8个电子。
然而,会留下一个氧原子,因为它需要2个电子。
在这种情况下,硫将能够向氧原子提供一个孤对,从而形成一个坐标共价键。
这就完成了共振结构,同时也满足了八隅体规则。
共振的第二结构
如上所述,硫磺有3个壳层,因此它有d轨道。
由于能够容纳超过8个电子,如果将坐标共价键去除,从而形成双键,则可以形成另一种共振结构。
在这种情况下,分子是中性的。
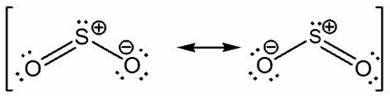
共振原因
可以从两种共振结构中判断出哪一种更准确。
我们已经测试了这两种结构,因此可以得出结论,实际结构可以在这两种结构之间绘制。
为了加深理解,我们可以说,二氧化硫有两个双键和一个半坐标共价键。
只有一个中间结构的存在因为共振结构不是不断变化的。
中间共振结构的原因
中间共振结构的根本原因是离域π键的存在。
由于π键的弱结构,它们能够离域,从而形成复杂的中间共振结构。
二氧化硫的VSEPR理论
为了详细地理解分子的几何结构以及它的键角和极性,了解价层电子对斥力理论是很重要的。
该理论表明,电子对有一种相互排斥的倾向,到电子排斥性最小的位置。因此,有些分子是直的,有些是弯的。
杂交过程也起着重要作用。在键的形成过程中,具有不同能量的轨道会自我退化,也会形成数量相近的相同轨道。
考虑二氧化硫(SO2)分子。硫原子和氧原子的1s轨道和2p轨道是杂化的。
SO2分子是弯曲的,不是直线的。这是SO2分子极性的主要原因,其中键的角度为120°,并包括三角形几何结构。
SO2分子不是线性的,电荷不能相互抵消,因此SO2形成极性分子。
类似的NO2分子也是弯曲的。请查看NO2几何.
二氧化硫的Sigma和Pi键
根据一个双共价键有1 sigma键和1 π键的共振结构,我们可以说SO2有2 sigma键和2 π键。
这可以归功于SO2拥有的2个双共价键,其中2个氧原子分别有一个单独的sigma和pi键。
SO2的酸性性质
SO2不是碱性的,本质上是完全酸性的。一旦溶解在水中,它就会开始与水分子反应,形成硫酸H2SO3。
So2 + h20—> h2so3
由于SO2是极性分子,容易溶于水,但硫酸(H2SO3)与硫酸(H2SO4)相比是弱酸。
二氧化硫作为氧化剂和还原剂
关于二氧化硫的另一个有趣的事实是,它既可以作为氧化剂,也可以作为还原剂。
在SO2中,硫由+4的氧化态组成,因此可以失去两个电子以达到+6的氧化态。
结果,二氧化硫既能得到电子又能失去电子,因此既能氧化又能还原剂。
二氧化硫的偶极态
在二氧化硫分子中,正如我们上面所讨论的,电负性有轻微的差异。
硫和氧原子之间的电负性差异以及SO2作为极性分子往往具有偶极态或矩。
因此,可以公平地说,在SO2中存在一个偶极矩或态,其值为1.61德拜。
结论
总结一下这个概念,我们现在可以理解二氧化硫(SO2)是一种无色气体,有轻微的刺激性气味,非常有害,可能导致窒息问题。SO2有一个共价键,因此这个分子可以被称为共价化合物。
SO2包括与一个氧原子的双键共价键以及与另一个氧原子的配位键。SO2由1s轨道和2p轨道杂化组成。由于分子二氧化硫的双共价键,它有2 sigma和2 π键。
SO2具有弯曲结构,本质上不是线性的。键角为120°的SO2成为极性分子,因为电荷无法相互抵消。二氧化硫溶解在水中形成弱硫酸H2SO3,其SO2本质上是酸性的。
极性分子SO2既是氧化剂又是还原剂,偶极值为1.61德拜。




