N2H4是联氨的化学式,联氨是一种无机化合物,也是一种氮化物。它也被称为重氮烷或二胺或氮氢化物,是碱性的。它是剧毒的,在聚合物泡沫的制备中主要用作发泡剂。
此外,它还用于制药和农化工业。
在这篇文章中,我们将研究N2H4的lewis结构,几何,杂化,以及它的lewis结构。
N2H4的Lewis结构
刘易斯点图或电子点结构是一种化合物分子式的图示,它的电子用点表示。
这些结构是以美国化学家吉尔伯特·牛顿·刘易斯的名字命名的,他在1916年提出了这种结构。
刘易斯结构说明了一个分子中不同原子之间的化学键,也说明了该分子中存在的孤电子对的数量。
这些是分子的电子结构及其原子键的表示,其中每个点表示一个电子,原子之间的两个点表示一个键。
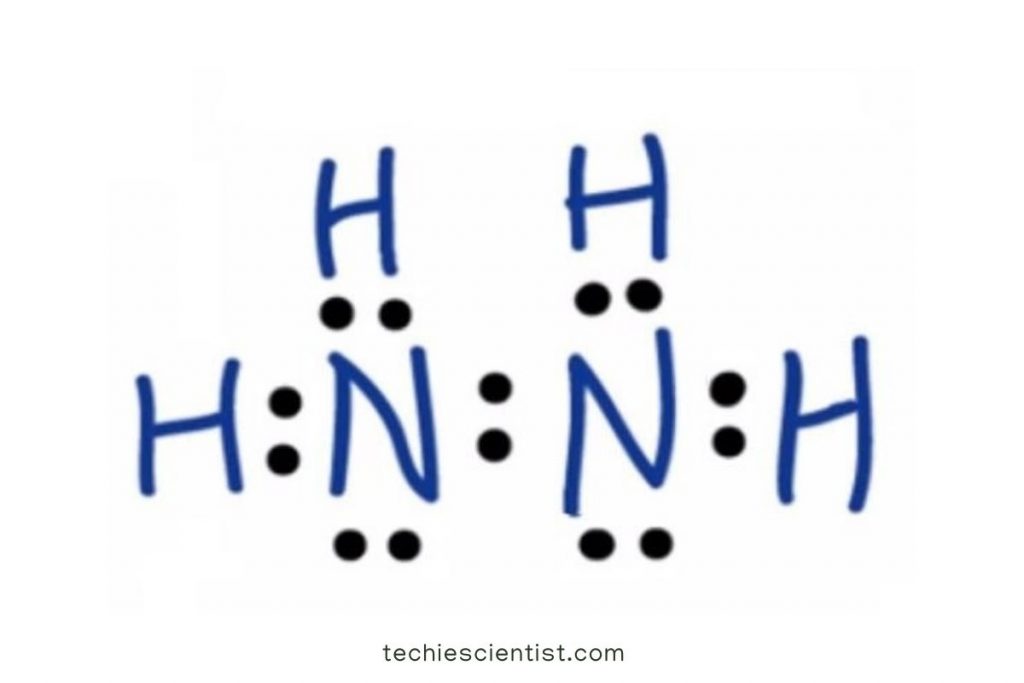
N2H4的Lewis结构如下。

我们已经知道,只有原子的价电子才能参与化学键,以满足原子的八隅电子。在N2H4中,氮有5个电子,而氢只有1个价电子。
在这里,必须指出的是,八隅体规则不适用于有两个电子的氢。
因此,每个氮原子与两个氢原子和另一个氮原子形成单键,从而满足所有参与原子的八隅体规则。
绘制N2H4的Lewis结构
绘制联氨刘易斯图应遵循以下步骤:
•首先,我们要计算分子中价电子的总数。
在这里,氮是第15族元素,因此,它的最外层有5个电子,而氢是周期表中只有一个价电子的第一个元素。
将所有原子的价电子相加,以确定一个分子N2H4中价电子的总数。
氮= 5个价电子;对于2个氮原子,2 * 5 = 10
氢= 1个价电子;对于4个氢原子,4 * 1 = 4
因此,N2H4的价电子总数= 14
•在此之后,我们将尝试通过将原子置于与单键连接的确定模式中来绘制刘易斯图的粗略草图。
这是为了给我们提供关于保持无界的电子数量的估计,以及任何原子完成它们的八隅体所需的电子数量。
•在这里,你可能会问N2H4分子中氮和氢分子的这种特殊序列的原因,即为什么氮原子被放在中心,即使氮的电负性比氢强。
实际上,氮原子需要三个电子来完成它的八隅体,而氢原子只需要把氮原子放在中心,就可以使分子对称,也可以使不同原子之间的电子共享更容易。
•从上面的结构可以清楚地看出,在与两个氢原子和另一个氮原子共享一个电子后,两个氮原子的八隅电子都得到了满足,因为它们各自都有一个孤对电子。
•因此,N2H4分子的最终结构是这样的:

•任何分子的刘易斯结构的准确性都可以通过计算该分子上的形式电荷来确定。
形式电荷是一个假设性的概念,被计算来评估推导的路易斯结构的稳定性。
•为了获得最大的稳定性,任何给定分子的形式电荷都应该接近于零。它是为一个分子的所有原子单独计算的。
形式电荷的计算公式如下:
形式电荷(FC) =[总数。自由态中价e -的量]-[总数无键e - - 1/2(总no。e -)]

•现在计算N2H4分子的形式电荷:
对于氮原子,自由态价电子总数= 5
非成键电子总数= 2
成键电子总数= 6
因此,氮原子的形式电荷= 5 - 2 - 1 / 2 (6)
= 0
对于氢原子,自由态价电子总数= 1
非成键电子的总数= 0
成键电子总数= 2
因此,氮原子的形式电荷= 1 - 0 -½(2)
= 0
•因此,N2H4分子上的总形式电荷变为零,表明推导的结构是稳定和准确的。
N2H4的几何
在价壳电子对排斥(VSEPR)理论中描述的假设被用于推导任何分子的分子几何。
根据这一理论,分子内不同原子的电子倾向于将自己排列得尽可能远,以便它们面临最小的电子间斥力。
分子内的所有电子,包括孤对电子,都产生电子间的斥力。然而,最大斥力存在于孤对-孤对之间,因为它们在空间中是自由的。
因此,分子的几何形状是由电子孤对和成键对的数量以及电子之间的距离和键角决定的。
此外,电子间的斥力决定了分子中键角的扭曲。
现在,为了理解N2H4的分子几何结构,我们将首先选择一个中心原子。
VSEPR理论假设一个分子的所有其他原子都与中心原子成键。由于两个氮原子都位于路易斯结构的中心,它们中的任何一个都可以被认为是中心原子。
因此,在N2H4的情况下,一个氮原子与两个氢原子和一个氮原子成键。
考虑到VSEPR理论,如果氮原子上的三个成键电子和一个孤对电子被放置得尽可能远,那么它必须获得三角金字塔形状。
通过AXN符号来观察N2H4的分子几何结构,其中A是中心原子,X表示附在中心原子上的原子数,N是孤对数。
因此,对于N2H4分子,这个符号可以写成AX3N,表示它具有三角锥体几何结构。N2H4分子的电子几何结构是四面体。
下表表示了不同分子的几何形状、键角和杂化,按AXN符号表示:
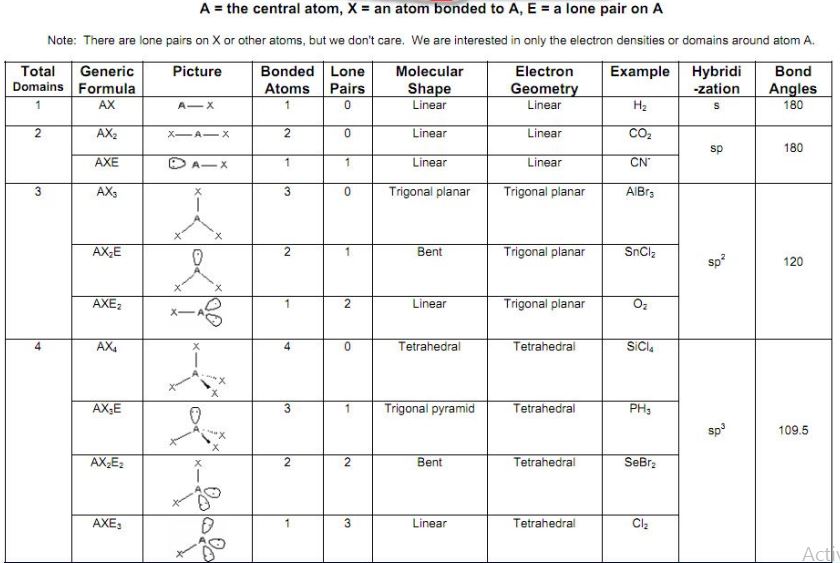
如上表所示,此处的键角为109.5°。N2H4分子的分子几何结构如下:
N2H4的杂化
杂化是将一个或多个能量相似的原子轨道混合,形成能量和形状与其组成原子轨道不同的全新轨道的过程。
这个概念最早是由莱纳斯·鲍林在1931年提出的。
由于原子轨道的混合而形成的杂化轨道以它们的基本轨道命名,即它们的名称表明了它们形成时所涉及的轨道。
例如,sp3杂化轨道表明它的形成涉及1个s轨道和3个p轨道。
任何分子的杂化都可以用下面给出的简单公式来确定:
杂化=中心原子上sigma (σ)键数+中心原子上孤对数
现在,用这个公式计算N2H4分子的杂化:
在这里,没有。键= 3
,没有。孤对= 1
因此,杂化= 3 + 1
= 4
因此,N2H4分子的杂化为sp3。
同时,如上表所述,具有三角锥体形状的分子总是具有sp3杂化,其中1个s轨道和3个p轨道以109.5°的角度放置。

N2H4的极性
一个分子中存在两个相反的电荷或极性,称为它的极性。
分子中产生这些电荷的原因是组成分子的原子之间存在的电负性差异。
在N2H4分子中,我们知道两个氮原子在同一个平面上,而且这两个原子之间没有电负性的差异,因此,它们之间的键是非极性的。
N2H4分子的极性是由氮原子和氢原子之间的电负性差异引起的。
比较N2H4分子中的两个氮原子,可以注意到它们具有相同数量的氢原子以及孤电子对。
然而,附着在一个氮原子上的氢原子位于垂直平面上,而附着在另一个氮原子上的氢原子位于水平平面上。
这导致在N2H4分子中形成净偶极矩。
此外,N2H4分子的形状被扭曲,因为不同原子之间的偶极矩不会相互抵消。
N2H4分子的净偶极矩为1.85 D,表明它是极性分子。

N2H4的性质
N2H4分子的重要性质如下表所示:
| 的名字 | 联氨 |
| 化学公式 | N2H4 |
| 颜色 | 无色 |
| 外观 | 发烟,油状液体 |
| 分子量 | 32.0452克/摩尔 |
| 密度 | 1.021克/厘米3. |
| 沸点 | 114°C |
| 熔点 | 2°C |
| 偶极矩 | 1.85 D |
| 杂交 | sp3. |
| 键角 | 109.5° |
| 溶解度 | 可溶于水 |
| 折射率 | 1.46044 |
N2H4的用途
联氨的一些重要用途如下:
•用于聚合物泡沫的制备
•它被用作空间飞行器的可储存推进剂,因为它可以储存很长时间。
•它被用作许多农药的前体。
•用于制药和农化工业。
•用于玻璃和塑料材料上的金属电解电镀。
•在冷却水反应堆中用作缓蚀剂。
•用作无机溶剂。
结论
N2H4分子的Lewis结构为:

路易斯结构上的形式电荷为零说明这是真实的结构。
N2H4分子的分子几何结构为三角锥体,电子几何结构为四面体。
N2H4的杂化为sp3。
N2H4分子的偶极矩为1.85 D。
希望你能理解N2H4的路易斯结构,几何结构,杂化和极性。如果你还有任何疑问,请在评论中问我。
学习快乐!看看我更有趣的帖子。




