我们都多次听说过“笑气”。但我们有没有试过了解更多关于这种能让人发笑的气体?我想没有!
在了解了一些关于笑气的知识后,决定分享给大家,下次大家就可以用知识来笑了!!
一氧化二氮通常被称为笑气。这种化合物还有其他几个名字,如甜空气、氮的氨氧化物等。
N2O是一种无色气体,分子量为44.013 g/mol。该化合物的沸点为-88.48℃,熔点为-90.86℃。
一氧化二氮,从用作火箭发动机的氧化剂到用于内燃机,在不同的领域有巨大的用途。它也被用于气溶胶推进剂。
现在让我们继续研究这种化合物的制备。
N2O制备方法
氧化亚氮的制备方法不止一种。一些方法是:-
工业方法在工业规模上,加热硝酸铵会产生一氧化二氮和水蒸气。
Nh4no3 - > 2h2o + n2o
实验室方法-氧化亚氮的制备也可以在实验室进行。加热硝酸钠和硫酸铵的混合物就得到了一氧化二氮
2 NaNO3 + (NH4)2SO4—> Na2SO4 + 2N2O + 4h2o
此外,氧化亚氮可以由尿素、硝酸和硫酸反应形成,
2 (nh2) 2co + 2hno3 + h2so4→2n2o + 2co2 + (nh4) 2so4 + 2h2o
奥斯特瓦尔德方法-氨与二氧化锰和氧化铋作催化剂氧化得到氧化亚氮。
这个过程被称为奥斯特瓦尔德过程。
2nh3 + 2o2 - > n2o + 3h2o
还有更多的反应用于制备N2O。除此之外,一氧化二氮也是地球大气的主要成分。浓度为0.330 ppm。
此外,硝化和反硝化是两种可以产生一氧化二氮的生物或自然过程。
现在,为了理解其他与N2O有关的反应,我们需要知道它的路易斯结构、杂化和成键。
那么让我们来逐个详细地讨论这些部分。
N2O路易斯结构
在进入一氧化二氮的路易斯结构之前,最好知道画路易斯结构的步骤。
如何画路易斯结构
刘易斯结构有助于我们了解化合物的结构、类型、键的数量、物理性质以及化合物如何与其他化合物相互作用。
画一个路易斯结构非常简单!
有一种常用的方法可以画出任何化合物的路易斯结构。看看下面记下的步骤:-
- 计算分子中价电子的总数。计算时一定要注意+号和-号。
- 选择一个中心原子;通常是键位最高的原子。
- 画一个只有单键的骨架结构。
- 用剩下的电子填满原子的八隅体。记住,从带电负性的原子开始,再到带电正性的原子。
- 如果需要,给出多个键来完成原子的八隅体。
- 最后,确保所有原子的形式电荷都尽可能低。你可以用下面的公式来计算:-

现在让我们找出N2O的路易斯结构,
原子的价电子为:-
- 氮= 5
- 2*氮= 5*2 = 10
- 氧气= 6
- 价电子总数= 16
接下来,我们需要决定中心原子。在这种情况下,具有最高键位的氮原子是中心原子。其中一个氮原子在中间。
在这之后,我们需要画出只有单键的分子的草图。下面附上的图片可以更清楚地解释这一点,

画完草图我们可以看到,剩下的电子是围绕着原子(结构1)给出的。这里,中间氮的八隅体没有实现。
所以在结构2中,一侧氮原子的孤对变成了中间氮原子的成键对。
但是,仍然缺少两个电子,使得另一对孤电子转换成键对。
因此结构3是笑气的最终路易斯结构。
正如在规则中提到的,我们可以看到在最终路易斯结构中的所有原子都有它们最低的形式电荷。请注意,其他两种结构的原子形式电荷都不是最低的。
现在让我们转向一氧化二氮的分子几何结构!
N2O分子几何
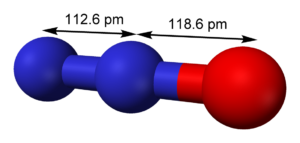
N2O的分子几何是线性的。

分子几何形状可以从VSEPR图确定。N2O与二氧化碳类似。它周围有两个原子,没有孤对。
因此该化合物是AX2型分子。
所以我们可以看到它有线性的分子几何和线性的电子几何。
电子几何和分子几何可能会有混淆。让我们把它清除掉!
分子几何结构只包括原子,而电子几何结构包括决定结构的所有电子对。
更简单地说,孤对包含在电子几何中,而不是分子几何中。
虽然N2O分子的形状是线性的,但原子间共享的电子是不平等的。电荷强度在分子上不均匀。
因此,它产生净偶极矩,被认为是极性分子。
从这个VSEPR图,我们还可以确定任何化合物的杂化。让我们进入下一部分来了解更多!
一氧化二氮杂化
在N2O中,氮原子是sp杂化的,氧原子是sp3杂化的。

N2O杂化的一种解释是末端的氮通过三键与另一个氮相连,因此它是sp杂化的。
下一个氮也是一样。氧原子与氮原子通过单键相连,因此是Sp3杂化的。
除了观察化学键,还有另一种方法可以确定杂化。
任何分子的杂化都可以用公式求出来。
H = 1 / 2 [v + m-c + a]
在这里,
H =杂交
V = No。价电子的
M = no。单价原子的
C=阳离子的电荷
负离子的电荷
若,H= 2 = Sp杂化
H= 3 = Sp2杂化
H= 4 = Sp3杂化
H= 5 = Sp3d杂交
H= 6 = Sp3d2杂化
这都是N2O杂化的结果。
接下来要讲的是一氧化二氮的分子轨道图。
N2O分子轨道图
分子轨道图描述了化合物中轨道的混合。
利用MO图,可以确定化合物的键序,从而使我们了解键长和键稳定性。
通过了解基本知识,一氧化二氮的MO可以很容易地画出来。
因此,我们来看看NO的MO

这里,左边是氮原子轨道(AO),右边是氧原子轨道(AO)。
中间是化合物NO的分子轨道。
在N2O的情况下,左边会有两个AO的氮。
这两个原子轨道将并排放置。氧化亚氮中的氧也会保持不变。
你可以通过结合ao来形成分子轨道。
结论
所以现在你终于可以对著名的“笑气”有一点了解了!!
这篇文章围绕着我们应该知道的关于一氧化二氮的基本化学。
在读完这篇文章后,你可以顺利地学习更多的反应和更深的知识。希望你喜欢这篇文章,如果你有任何问题,随时可以问我!




