SF6或六氟化硫是一种无机气体,是化学中已知的最稳定的气体之一。这种气体的密度比空气大。由于这种气体在本质上是无味无色的,所以无法进行一般的鉴别。气体本身也没有味道。
SF6在性质上是不燃不燃的。然而,在极端的高温和高压下,它可能会从储存容器中爆裂,飞向空中。
SF6可与少数化合物反应进一步解离并参与后续反应。
Sf6 + 4h2o—> h2so4 + 6hf
SF6与水结合形成硫酸和氟化氢。
SF6 + 8NaOH—> Na2SO4 + 6NaF + 4H2O
SF6和氢氧化钠反应生成硫酸钠,氟化钠和水。
此外,SF6不易溶于水,可溶于非极性有机溶剂。
对人类的影响:
这种气体被人吸入后会转移到肺部,任何形式的皮肤或眼睛接触都可能导致冻伤。
下面是SF6不同性能的markdown。
- 分子量:146.06克/摩尔
- 沸点:-63.8摄氏度
- 熔点:-83华氏度
这种气体以液化气体的形式被自身的压力压缩来运输,但不需要任何特殊的处理或储存。
SF6 Lewis结构
通过学习任何化合物的刘易斯结构,我们深入了解了幕后的工作原理。
化学键的性质,化学键的类型,以及化学键的形状,这些都是我们在研究化合物的路易斯结构时要讲的。
要做出路易斯结构,你需要彻底了解八隅体规则、价电子和孤对的基本概念。
你们还记得这些术语吗?
好吧,如果没有,那就让我们一起修改吧。
价电子简单地说,价电子可以定义为存在于原子外层的电子。
这些电子分布在不同的能级,即s、p、d和f。价电子在决定原子的各种性质方面非常重要。
八隅体规则:每个原子都试图遵守八隅体规则以变得稳定。最外层需要8个电子才能稳定。
这就是每个原子都试图通过与相邻原子成键来达到的目的。这就是不同的化合物是如何形成的具有不同的化学和物理性质。
现在回到SF6的路易斯结构,让我们找出价电子,然后画出最终的路易斯点结构。
SF6中的价电子
SF6中有两种原子,硫和氟。
有一个硫原子,而氟原子有6个。
让我们通过了解硫和氟的价电子来开始构造路易斯结构。
硫的价电子= 6,氟的价电子= 7
这个化合物中有6个氟原子,所以氟的总价电子= 7*6 = 42个价电子
因此,SF6的总价电子为= 42+6 = 48
你有没有想过为什么硫的价电子是6?
好吧,如果是,那么让我们给你答案。
硫的原子序数是16。这些是存在于这个元素中的电子总数。如果我们开始用电子排布的方法填充这些电子那么我们就会有如下的排列,
1s2 2s2 2p6 3s2 3p4
在最外层,我们有6个电子,在氟原子的例子中也被称为价电子。
SF6的Lewis点结构
中心原子是硫,因为它的电负性比氟小。这是因为氟的外层有5个电子,它需要多一个电子才能达到稳定,这更容易实现。
由于有6个氟原子,硫和氟之间会形成6个键。硫原子和氟原子共用6个电子。
这里有一个相同的图像表示。
键的形成由一条直线表示,孤电子对由每对电子对的两个点表示。
现在,当我们知道有多少键形成了,让我们看看有多少孤对会形成。
当6个键形成时,12个电子会被用掉,剩下36个价电子。
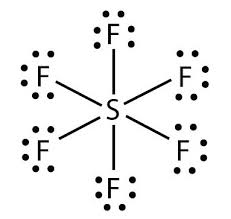
你看到硫的外层有超过8个电子了吗?
这样做的原因是一些原子可以膨胀它们的价层。当最外层能容纳更多电子时就会出现这种情况。
剩下的电子是氟原子上的孤电子对。每个氟原子上,都有3对孤电子。
所以会有18对孤电子,总共36个电子。
氟原子的八隅体是完整的,硫原子是个例外,它的八隅体是扩展的。
这就是SF6的路易斯结构,现在让我们看看化合物的杂化和分子几何结构。
SF6的杂化
路易斯结构是键形成的一种表示形式。但是如果你想了解一个化合物在平面上的样子那么我们就需要找到它的杂化和进一步的分子几何结构。
这是电子如何被填入不同能量轨道的图示。
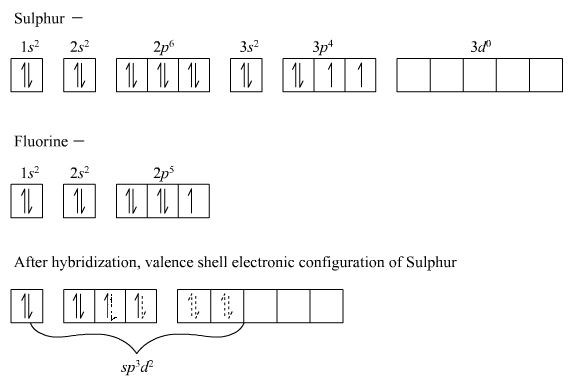
硫的总电子数为16,因此壳层根据其容量和层次水平被填充在不同的能级。因此,硫的基态杂化为3s2 3p4。
对于氟,基态杂化是2s2 2p5。
现在,当这两个原子结合在一起化合物进入激发态硫的电子从p能级移动到d能级。
因此,构型就变成了sp3d2。因此,SF6的杂化为sp3d2。
这是因为硫可以膨胀它的价层来形成键以达到稳定。
SF6的分子几何和MO图
硫原子周围都是氟原子这使得化合物在平面上看起来很对称。
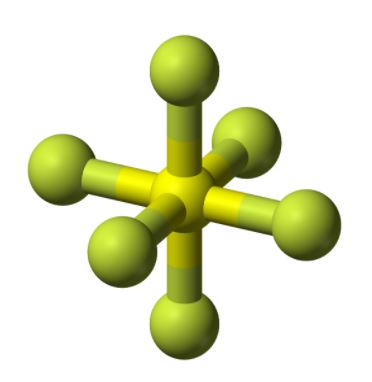
当我们观察任何化合物的分子几何结构时,我们都能看到原子如何分布的三维图像,这是我们在制作刘易斯结构时无法识别的。
借助分子几何,我们也可以找到键角。对于SF6,键角是90度,因为原子均匀地分布在中心原子硫周围。
你可以借助VSEPR理论找到化合物的形状。该理论涉及电子斥力和化合物形成某种形状以达到稳定。
在SF6中,硫和氟之间有6 sigma键,每个氟原子上有3个孤对。这些孤电子相互排斥,并在中心原子周围保持对称性。
这就是为什么SF6的形状是八面体,这也可以被称为它的分子几何形状。
下面是SF6的MO图。

你可以观看这个视频来学习如何一步一步地制作MO图。
SF6的极性
当我们深入研究化合物的结构和性质时,化合物的极性是一个主要的讨论话题。
SF6的电荷分布基本一致,使其偶极矩为0。由于对称排列,偶极矩被抵消了。
这使得SF6本质上是非极性的。
你还必须参考文章上写的SF6极性。
结论
当我们来到这节课的最后,让我们看看到目前为止我们在这篇文章中学到了关于SF6化合物的知识:
- SF6是一种无色无味的气体,在自然界中不燃不燃。
- 中心原子是硫原子和6个氟原子成键。
- 路易斯点结构有6 sigma键,孤对在氟上。
- SF6的杂化为sp3d2。
- SF6具有八面体分子几何结构,本质上是非极性的。
我们希望你在阅读这个有趣的化合物时玩得开心。
如果您有任何疑问,您可以联系我们,我们很乐意为您解惑。
谢谢你的阅读。




