XeF2是由惰性气体氙和卤素氟形成的共价无机卤化物。这是一种活性溶剂,被发现可溶于不同的氟化物,如HF和五氟化溴。
如果我们看一下二氟化氙的合成过程,方程式如下:
Xe + F2—热—> XeF2
XeF2作为氧化剂和氟化剂,用于氧化不同的碳氢化合物,包括芳香族化合物和无环化合物。
不仅如此,这种氟化物还可以用来蚀刻硅,形成四氟化硅(SiF4),而不需要任何外部能量的应用。
如果你想知道XeF2是什么样子的,它看起来是一种无色至白色的晶体固体,密度约为4.32 g/cc。
这种卤化物会导致一些严重的危险,如皮肤烧伤和严重的眼睛损伤。不仅如此,如果吸入或吞下,它是致命的。
化学成键
当两个或两个以上的原子聚集在一起时,它们发生反应并结合形成同质和异质分子。分子的形成是通过某些键的产生来实现的,这些键根据原子的强度将它们结合在一起。
这被称为化学键,它是定义给定分子化合物的内部结构和性质的基础,包括它所表现出的性质(物理和化学)。
在我们在本文中直接进入XeF2的化学键之前,我们希望您学习并概括一些重要的术语和概念。
价电子
当我们学习化学键时首先要学习的是价电子的概念。价电子是决定原子价的最外层电子。
如果你仔细看周期表,这些基团会帮助我们找出某个原子元素的价电子数。
例如,碳在第4族(也称为XIV族),因此价电子层由4个电子组成。
Lewis结构
刘易斯结构,也称为电子点结构,是化学键的一个基本模型,我们使用价电子的概念来粗略地描绘给定分子的二维图形。
我们用点来表示外层电子,用线来表示键类型。
氙是惰性气体元素。因此,它有8个价电子。氟是属于第七族的卤素,因此它的价是7。
总价电子数=8 + 7*2 = 22
如果你看元素周期表,我们知道氙的电负性比氟小,因此它会占据中心原子的位置。
现在我们有了中心原子和总价电子数,我们将找出电子如何定位以达到八隅体构型(即每个原子的外层有8个电子)。

现在,正如我们所看到的,我们已经实现了XeF2内部的三个原子的八隅体实现,单键的形成已经完成。
但是如果你数一下图中的价电子总数,我们可以看到这些点加起来是20个而不是22个。
现在,最明显的选择是用剩下的两个价电子形成双键而不是单键。
氟的电负性很强,通常不会形成双键。所以,我们保持氙周围的价电子,然后计算形式电荷。
形式电荷
如果我们假设每个电子都被原子平均占有,我们就可以给一个原子分配一个形式电荷。
这对于化学键来说是一个必要的话题,特别是对于Lewis结构的确定,我们需要检查每个结合原子的最小形式电荷,以得到完美的图表表示。

对于Xe,形式电荷= 8(价电子数)- 0.5*4(成键电子数)- 6(孤对电子数)= 0
对于每个氟原子,形式电荷= 7 - 0.5*2 - 6 = 0
因此,由于这两个元素的形式电荷值都是最小的,我们就得到了最合适的路易斯结构。
注意:这是八隅体规则的一个例外,因为氙在其价壳层云中有超过8个电子。
分子几何
如果你想深入了解分子内部是什么样子的,我们需要学习分子几何。
这是一个从2D到3D结构表示的跳跃,我们可以直观地描绘出一个分子是如何在现实中保持成键状态的。
在这里,为了帮助我们确定正确的分子形状以及键长和角度,我们使用了一种称为价壳电子对排斥模型(VSEPR)的理论。
该理论处理原子核周围的负电子云之间发生的类似电荷排斥,并将它们最小化以获得接近稳定的化合物。
氙是一种稀有气体,属于第8族(第XVIII族),不倾向于形成化学键。在XeF2中,它作为中心原子同时也和两个氟原子形成了两个单键。
现在,我们已经讨论了分子几何可以通过VSEPR理论预测。让我们看看这张图:

这里我们可以根据分子的空间位数和孤对数找到不同形状的分子。
通过Lewis结构我们可以看到XeF2中的氙有三个孤对。
对于空间位数,我们需要加上中心Xe和孤对电子的键合原子数。
因此,Xe在二氟化氙中的空间数= 3+2 = 5。
如果我们看图片,我们可以发现它的形状是线性的键角是180度。
如果我们详细讨论,我们可以说,为了使电子斥力最小化,这样的结构就形成了。单键起初使结构呈线性。
接下来是每个孤对,它们将侧向原子从Xe推向一定程度。最后,所有三个孤对的综合影响使合成结构呈线性。

杂交
原子有一个叫做原子轨道(AO)的概率函数,它让我们知道组成电子的位置。我们有s p。D f原子轨道。
你知道aoo不会在分子内形成键吗?
它们融合形成所谓的杂化轨道(例如sp, sp3),在化学中参与成键。
这个过程被称为杂交。
如果我们要学习二氟化氙的杂化,我们就必须研究它们各自的电子构型。
Xe: 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6
或者,Xe: [Kr] 4d10 5s2 5p6
F: 1s2 2s2 2p5
或者,F:[他]2s2 2p5
我们可以看一下XeF2分子中所有原子的轨道。
现在,我们要找出哪个AO和另一个AO结合形成杂化轨道。
现在,根据路易斯结构,氙的价电子层(未成对)有8个以上。这使得原子被激发,构型现在是5s2 5p5 5d1。
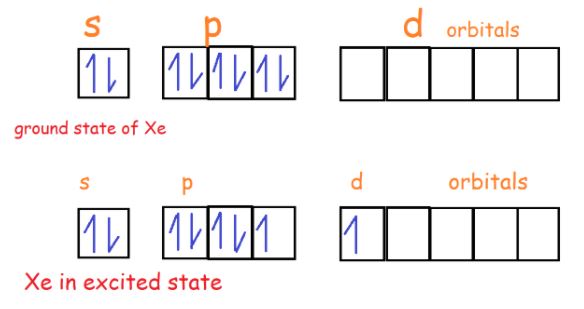
杂化轨道是sp3d。在XeF2 (F-Xe-F)中,两个杂化轨道用于sigma键形成(单键)。
分子轨道图
如果我们进一步研究化学键和杂化,我们就会了解分子轨道理论,这是量子力学的一个概念。
这给了我们一个关于MO图的想法我们不考虑线性键。相反,我们研究的是恰好在原子核影响下移动的电子的空间和能量特性。
在这里,我们涉及成键和反键轨道,sigma和π键以及HOMO(最高占据MO)和LUMO(最低未占据MO)的概念。
XeF2是一个多原子分子。因此,我们有很多原子轨道要处理,这就产生了大量的mo。
在XeF2中,Xe周围有10个电子,这可能导致共振和离域成键。
然而,当我们研究分子轨道理论时,我们可以看到二氟化氙有8个充满的MOs:
2 bonding and non-bonding orbitals each, and 2 π bonding and anti-bonding orbitals each.
MOs的混合导致了反键轨道的形成,我们得到了11个填充的分子轨道,同时,我们知道XeF2遵循3中心4电子键模型。

结论
二氟化氙是一种稀有气体高价卤素化合物,但在八隅体规则中有一个例外,没有净偶极矩。
要了解不同的性质和特征,对化学键有一个概念是很重要的。本文讨论了XeF2的Lewis结构、分子几何、杂化和基于分子轨道理论的图。现在,是时候让你们看一遍,更好地理解化学了。
学习快乐!




