二氟化氙是一种无机化合物,化学式为XeO2F2.其分子量为201.289 gm,由六氟化氙部分水解而成,反应如下:
XeF6+ 2 h2O——> XeO2F2+ 4高频
你好朋友!这是另一种有趣的化合物。在本文中,我们将讨论XeO的各种属性2F2.
所以,继续读下去……
价电子
原子中的电子围绕它的中心(也就是原子核)旋转。每个电子都带一个负电荷,并具有与之相关的特定能量。
电子的能量随着电子远离原子核而增加。因此,在原子中,离原子核最远的电子具有最高的能量,被称为价电子。
价电子层,也就是最外层,容纳了参与化学键的价电子。
八隅体规则
如前所述,原子利用价电子形成化学键。然而,由原子形成的键的数量和类型也取决于这些电子存在于最外层。
通常,每个原子都试图获得离它最近的惰性气体的电子排布,从而变得稳定。
因为所有的惰性气体,除了氦,在最外层都有8个电子,所以其他元素的原子也试图在价电子层获得8个电子。这就是所谓的八隅体规则。
这个概念是由沃瑟·科塞尔和吉尔伯特·n·刘易斯提出的,并奠定了与原子相关的所有其他概念的基础,即杂化、分子几何等。
Lewis结构
一个原子的路易斯结构是它的原子核和价电子的原子结构的简化表示。它说明了原子中电子的排列方式。
在这里,电子用点表示,原子核用原子符号表示。两个原子之间的键用一条线表示。
XeO2F2的Lewis结构为:

观察XeO2F2的Lewis结构,可以看出所有的原子都达到了它们的八隅体。
氙是惰性气体,已经有8个价电子。另外,原先缺少1个电子的氟原子和缺少2个电子的氧原子也都得到了稳定的八电子体。
然而,你可能会问,如果氙已经有8个电子了,为什么它还能和其他原子成键呢?
你是对的,这对大多数原子来说是不可能的。然而,氙和其他惰性气体是一个例外,因为它们有空的d轨道来容纳额外的电子。
氙可以扩展其八隅体,并在其价壳层中容纳超过8个电子,这是因为存在空的5d轨道。
绘制XeO2F2的Lewis结构
现在我们将逐步画出XeO2F2的Lewis结构:
•首先,我们将计算XeO2F2分子中每个原子的价电子数。
对于18族元素氙,
价电子数= 8
氧,第16族元素,
价电子数= 6
因此,对于2个氧原子,总价电子数为e- - - - - -= 12
同样地,对于第17族原子氟,
价电子数= 7
因此,对于2个氟原子,总价数为e- - - - - -= 14
因此,对于XeO2F2分子,
价电子总数= 34
•现在,我们将为这个分子选择一个中心原子。通常,电负性最小和最稳定的原子被选择用于此目的。
在目前的情况下,选择氙作为最稳定的原子作为中心原子。
•接下来,我们将用单键将所有参与原子连接到中心原子。
这是为了评估参与的原子是否需要更多的电子。如果是这样,那么进一步的安排将完成它的八隅体。

•从上图可以清楚地看出,氙和氟原子的八隅体是完整的。
然而,每个氧原子仍然需要一个额外的电子,这可以通过在氙和氧原子之间形成双键来提供。
•在这一步之后,所有参与原子的八隅体都完成了,中心原子只剩下4个键对和一个孤对。
•因此,XeO2F2的最终lewis结构如下所示:
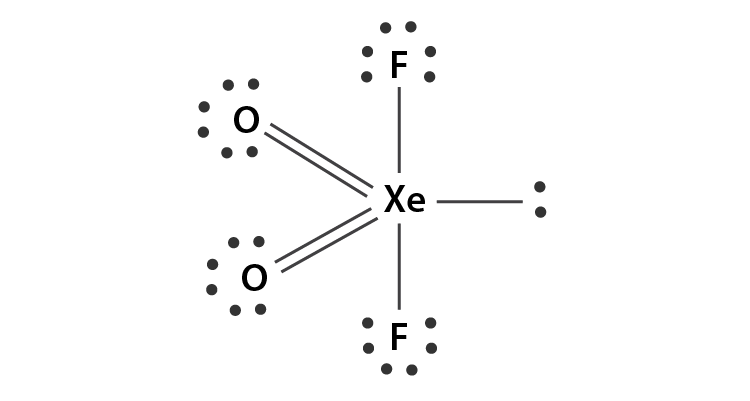
形式电荷
计算分子的形式电荷来评价其路易斯结构的稳定性。虽然,这是一个假设的概念,但帮助我们确定我们的推导结构的正确性。
它由公式给出:
形式电荷(FC) =价电子数- - - - - -原子中-非的数目结合e- - - - - -- 1/2(成键数e- - - - - -)
分子的形式电荷为零表示稳定。
现在我们将通过计算XeO2F2分子中每个原子的形式电荷来计算它的形式电荷。
对于氙原子
价电子数= 8
非成键电子数= 2
成键电子数= 12
因此形式电荷= 8 - 2 - 1 / 2 (12)= 0
对于氟原子
价电子数= 7
非成键电子数= 6
成键电子数= 2
因此,形式电荷= 7 - 6 -½(2)= 0
对于氧原子,
价电子数= 6
非成键电子数= 4
成键电子数= 4
因此形式电荷= 8 - 4 - 1 / 2 (4)= 0
因为每个原子的形式电荷都是零。因此,XeO2F2分子的总形式电荷也变为零。
因此,上面所画的XeO2F2分子的Lewis结构是正确的。
XeO2F2的分子几何结构
利用价壳电子对(VSEPR)理论的假设预测了化合物的分子几何结构。
该理论指出,分子的几何形状取决于分子中心原子上的键对和孤电子对的数量。
基本上,这个想法是所有的电子都带负电荷,并且像电荷一样互相排斥这些电子也互相排斥。这种排斥力的程度可以通过VSEPR理论来确定分子的形状。
VSEPR理论进一步指出成键电子对和非成键电子对之间的排斥程度是不同的。由于非成键电子可以自由移动,这些电子之间的斥力最大。
此外,由于成键电子已经被绑定到两个原子上,运动自由受到限制,因此这些电子之间的斥力被最小化。
因此,任何分子都有两种几何形式。一种是基于成键原子预测的电子几何,另一种是分子几何,它也考虑了孤对电子在决定分子几何中的作用。
基于VSEPR理论,我们可以通过计算分子中心原子上的键对和孤电子对的数量来确定分子的电子几何结构和分子几何结构。
以XeO2F2为例,我们已经计算出中心原子,即氙原子,有4对键电子和1对孤电子。
现在,我们可以确定XeO2F2的几何形状,通过基于VSEPR理论假设的图表,如下所示。

因此,XeO2F2分子的电子几何结构为三角双锥体,而该分子的分子几何结构为跷跷板。而且,不同原子之间的键角是91o, 105年o、174o,分别。

XeO2F2杂交
当一个分子形成时,能量相似的轨道也会结合形成一个完全不同的轨道。这个过程被称为杂交,是由莱纳斯·鲍林在1931年首次提出的。
VSEPR理论指出,分子的杂化可以通过以下公式给出的空间数来计算:
空间没有。=中心原子上的sigma (σ)键数+中心原子上的孤对数
因此,对于XeO2F2分子的空间位数可由上式计算,如下:
XeO的空间数2F2分子= 4 + 1 = 5
我们现在可以通过使用下表确定XeO2F2分子的杂交状态:
| 位的数量 | 杂化状态 |
| 1 | 年代 |
| 2 | sp |
| 3. | sp² |
| 4 | sp³ |
| 5 | sp³d |
| 6 | sp³d² |
因此,XeO的杂化态2F2分子是sp3.D或DSP3..
此外,我们可以通过观察成键电子在中心原子轨道上的调节来确定杂化态。
以XeO为例2F2分子,我们知道氙原子的杂化态是sp3..然而,作为惰性气体,它仍然有一个空的d轨道可供支配。因此,基态下氙原子的杂化可以写成:

在激发态,p电子跃入d亚壳层,杂化可以写成:

这四个被激发的电子与两个氧原子和两个氟原子成键,剩下的两个电子是孤对电子。因此,XeO2F2的杂交状态分子是sp3.d.

XeO2F2的极性
在XeO2F2分子中,极性的存在是由于参与原子之间的电负性差异。
氙原子的电负性为2.6,氧原子的电负性为3.44,氟原子的电负性最高,为3.98。
因此,由于这个分子中所有的键都是极性的,而且它的形状不对称,因此偶极矩没有被抵消,XeO2F2分子是极性的。
结论
XeO2F2分子的Lewis结构为:

XeO的电子几何2F2分子为三角双锥体,分子几何形状为跷跷板。
XeO的杂化状态2F2分子是DSP3..
XeO2F2分子是极性的。




