盐酸是一种无色有刺激性气味的液体。用化学式HCl表示,即它含有一个氢原子和一个氯原子。它也被称为盐酸。在工业上,盐酸是由氯化氢与水反应而制得的。
在人类和其他一些动物的胃中,它也被发现是胃酸的组成部分。它被用于许多无机化合物的生产,在钢铁的酸洗,在pH控制和中和反应等。
嘿,读者! !欢迎阅读另一篇关于技术科学家的新文章。万博网页版
在这篇文章中,你将学习你需要知道的关于盐酸分子间作用力的一切。
所以请继续阅读....
盐酸中存在哪些类型的分子间作用力?
盐酸分子间存在偶极-偶极相互作用和伦敦色散力。
由于氢(2.2)和氯(3.16)的电负性不同,氢原子上产生了轻微的正电荷,而氯原子则获得了轻微的负电荷。一个分子的微带正电的氢原子和另一个分子的微带负电的氯原子之间产生的引力被称为偶极-偶极相互作用。
伦敦色散力发生在所有分子之间。

为什么盐酸的沸点很低?
在盐酸分子中,氢原子和氯原子通过极性共价键结合。这个键的形成是由于氢和氯之间的电负性差异,这是由于分子内部形成了两个独立的极点。
电负性更强的氯原子通过将共享电子对拉向自己而获得部分负电荷,而氢原子则获得部分正电荷。
因此,在同一个分子中形成两个相反的电荷或极点,也称为偶极子。
当一个分子的带正电的氢一端与另一个分子的带负电的氯一端接触时,分子间的引力就出现了,这被称为偶极子-偶极子相互作用。
盐酸分子间存在的另一种分子间作用力是伦敦色散力。这些力实际上存在于所有分子之间,当我们讨论HCl中的分子间成键时,这些力并不重要。
因此,HCl分子之间唯一相关的分子间作用力是偶极子-偶极子相互作用,与其他各种化合物中存在的其他类型的分子间作用力相比,强度相当弱。
不同分子间作用力的强弱顺序如下:
离子-离子>离子-偶极子>氢键>偶极子-偶极子>偶极子-诱导偶极子>诱导偶极子-诱导偶极力
化合物的沸点取决于化合物中分子间作用力的强度。大多数情况下,离子化合物具有很强的分子间键。
看一下HCl分子,它是一种通过极性共价键结合的非离子化合物。此外,作用于该化合物的唯一分子间力是偶极子-偶极子相互作用。
因此,由于其分子之间的分子间键较弱,HCl具有较低的沸点。

分子间作用力的类型
分子间作用力是指存在于同一化合物的相互靠近的不同分子之间的吸引力。例如,偶极-偶极相互作用,氢键等。
它们不同于存在于同一分子的两个或多个原子或离子之间的分子内引力。例如离子键、共价键等。
不同类型的分子间引力描述如下:
离子-离子力:这是离子化合物分子间产生的静电力。当不同分子中带相反电荷的离子相互靠近时,就会产生离子-离子力。
•离子偶极力:这些力存在于极性分子和离子分子之间。极性分子的原子上有部分正电荷和部分负电荷。
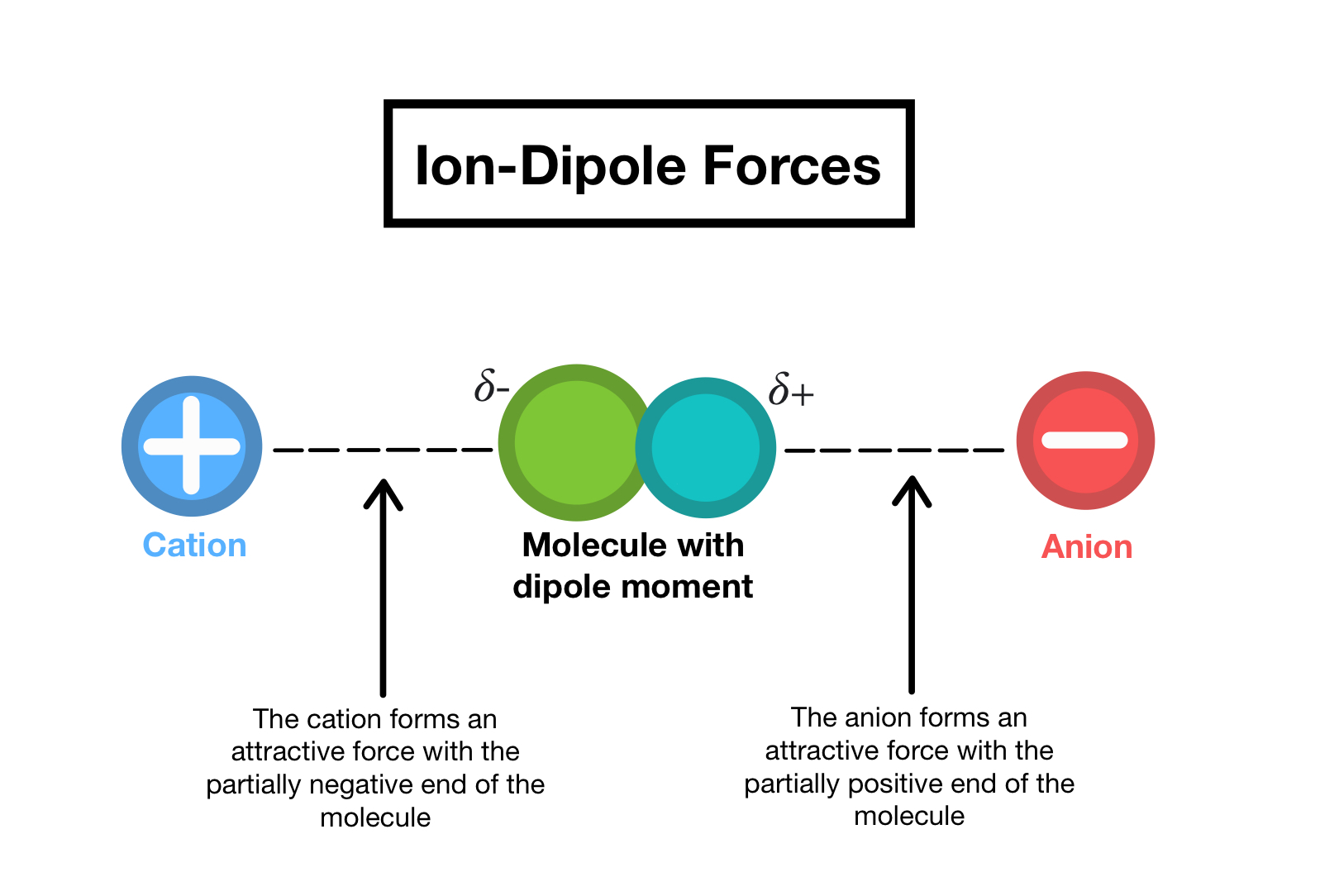
例如,当NaCl或KCl溶解在水中时,它们的离子与H的极性分子结合2这些相互作用的强度取决于极性分子的大小和偶极矩。
•偶极-偶极相互作用:这些相互作用发生在具有永久偶极矩的极性分子中。当这些分子与其他类似分子相互作用时,它们就形成了偶极-偶极相互作用。
分子的极性是由键合原子的电负性不同决定的。例如,在盐酸的情况下,氢原子获得部分正电荷,而氯原子上产生部分负电荷。

•氢键:这也可以被认为是一种偶极-偶极相互作用,因为它们是由于分子原子之间的电负性差异而产生的。
具体来说,氢键只发生在氢与高电负性原子(如氮、氧和氟)结合的分子中。
看看下面的文章

•伦敦色散力:这些也被称为诱导偶极子-诱导偶极子力。这是存在于所有类型分子之间的最弱的分子间作用力。
当分子内的电子移动时,会产生暂时的正电荷或负电荷,这也称为感应电荷。
当这些诱导电荷与另一个分子带相反电荷的一端相互作用时,就会发生诱导偶极子-诱导偶极子相互作用。
看看这篇文章CH4分子间作用力.

为什么氢键在盐酸中不发生?
氢键存在于分子之间,其中氢与高电负性原子(如氮、氧和氟)共价键。
由于原子的电负性差异很大,部分正电荷在氢原子上形成,部分负电荷在电负性原子上形成。
一个分子的氢原子和另一个分子的电负性原子之间产生静电吸引。
这些引力的强度主要取决于原子之间的电负性差异以及原子之间的大小差异。
氢键的强度随分子间电负性差的增大而增大,随原子大小差的增大而减小。
例如,在HF的情况下,NH3.,或H2O,氟原子、氮原子和氧原子的大小相对较小,因此这些分子中可能形成氢键。
然而,对于HCl,虽然电负性的差异很容易,但氯原子的尺寸很大,因此电子密度很低。因此,这个分子不能形成分子间氢键。
盐酸有偶极矩吗?
分子的净极性被称为偶极矩。极性是由于结合原子的电负性不同而产生的。因此,分子的偶极矩也随着电负性差的增大而增大。
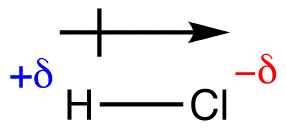
在鲍林尺度上,氢原子的电负性值为2.3,而氯原子的电负性值为3.16,表明电负性差异很大。
因此,HCl的偶极矩为1.03德拜。
常见问题
问:分子间键对物质的性质有什么影响?
答:分子间作用力影响物质的沸点和冰点。通常,物质的沸点和冰点随着分子间作用力的增加而增加,反之亦然。
问:为什么HCl在所有卤化氢中沸点最低?
答:在卤化氢中,HF具有最高的沸点,这是由于其分子之间存在氢键。在其他卤化氢中,HCl含有偶极-偶极相互作用,而溴和碘分子的电负性不强,不能使分子极化。
然而,这些原子中的电子数量比氯原子多,因此它们表现出更强的范德华力。这些力在HI中最高,在HCl中最低。
因此,卤化氢的沸点按以下顺序增加:
HCl < HBr < HI
问:为什么HCl的熔点比NaCl低?
答:盐酸分子具有简单的线性结构,分子间通过弱分子间作用力连接。由于物质的熔化依赖于分子间作用力的破坏,盐酸很容易克服它们。
然而,NaCl是一种离子化合物,其中的分子通过离子-离子相互作用结合在一起,这种相互作用非常强。因此,NaCl的熔点比HCl高。
相关的话题
盐酸的性质
氯化氢的几个重要性质如下:
•在室温和常压下,它是一种透明气体,用化学式HCl表示。
•盐酸的分子量为36.458 gm/mol。
•HCl的熔点和沸点取决于水溶液的浓度或摩尔浓度。
•HCl在189 K液化,在159 K温度冻结。
•它是一种强腐蚀性的单质子酸。
结论
偶极-偶极相互作用和伦敦色散力作为分子间引力存在于盐酸分子之间。
HCl分子之间的偶极-偶极相互作用是由于氢原子和氯原子的电负性不同而产生的。
不同分子间作用力的强弱顺序如下:
离子-离子>离子-偶极子>氢键>偶极子-偶极子>偶极子-诱导偶极子>诱导偶极子-诱导偶极力
盐酸偶极矩为1.03德拜。
快乐学习! !




