氯化铵是一种白色结晶盐。易溶于水,呈弱酸性。NH4Cl自然地以一种矿物的形式存在,被称为sal氨,在一些火山喷口附近也有。
综合来说,它是HCl和氨反应的产物,也是索尔维工艺的副产物。氯化铵主要用作肥料,但也用于医药、食品、实验室、电池等。
所以是NH4Cl离子还是共价?
氯化铵是一种离子化合物。在北半球4Cl,金属(氯)和多原子离子(NH)之间的键4就形成了。金属原子与多原子离子之间形成的键本质上是离子键。因此,它是一种离子化合物,其中氨分子将一个电子捐赠给氯原子,形成NH4+离子和氯- - - - - -分别离子。
然而,氮和氢原子之间的键本质上是共价键,因为它们是通过共享电子形成的。有些书也考虑了NH中的化学键4Cl分子是配位共价键。

什么是离子化合物和共价化合物?
正如名称所示,离子化合物是原子通过离子键结合的化合物,而在共价化合物中,原子通过共价键连接。
但是,这些化学键是如何形成的?
原子与其他原子形成键来稳定自己。
当参与的原子共享电子时,共价键就形成了,即两个原子都可以使用所有的电子,作为价壳层的成员,参与成键,并稳定自己。
通常,两种非金属之间会形成共价键。此外,所涉及的原子具有相同或相似的电负性。
共价化合物是电的不良导体,熔点和沸点低,通常在室温下以液体或气体的形式存在。
共价键又可分为极性共价键和非极性共价键。
当电负性差在0.4和1.6之间时,形成极性共价键。在这种情况下,电子会稍微向一个原子移动。这导致在这个原子上产生一个轻微的负电荷,在另一个原子上产生一个轻微的正电荷,分别记为δ+和δ-。例如,H2O, CH4等。
在非极性共价键中,电子在参与的原子之间平等地共享。比如Cl2阿,2,等。
另一方面,当参与成键的电子对完全转移到其中一个原子时,离子化合物就形成了。这些是由于静电吸引而形成的电价键存在于两个相反的电荷种之间。
实际上,离子化合物是由一个阳离子(带正电的离子)和一个阴离子(带负电的离子)组成的。然而,化合物的净电荷是中性的。
通常,离子键是在金属和非金属之间或金属和多原子之间形成的。参与成键的原子的电负性有很大的差异,通常大于1.6。
它们相对更稳定,熔点和沸点高,是电的良导体,通常在室温下以固体形式存在。
例如,在NH的例子中4Cl, NH4+表现为阳离子,而Cl- - - - - -起到阴离子的作用。

为什么NH4Cl是离子型的?
氯化铵是一种离子化合物,因为在这种情况下,金属氯和多原子氨之间形成了键。
在前一节中,我们研究了离子化合物是当多原子与金属结合时形成的。因此,NH4氯是离子化合物。
氯化铵是氨和氯化氢反应形成的。由于氨已经是一种稳定的化合物,其中氮原子各从三个氢原子获得一个电子,所以它不需要任何其他的电子。
因此,当它与HCl反应时,氢原子会附着在氨上,从而形成离子化合物。
北半球4Cl分子的电离过程如下:
(NH4+] [Cl- - - - - -]
此外,根据IUPAC,所有的盐都至少由一个阳离子和一个阴离子组成。在北半球4Cl是一种盐,是一种离子化合物。
电负性
原子的电负性是衡量原子在成键过程中把电子拉向自己的能力。
电负性较强的原子能够容易地吸引电子对,从而获得一个负电荷,而另一个原子获得一个正电荷。
原子的电负性是用鲍林尺度来测量的。氟是迄今为止已知的电负性最强的元素。
氟在鲍林标度上的电负性值是4。另一方面,钫和铯的电负性值最低,接近0.7。
参与成键的两个原子的电负性差异越大,共用电子所受的拉力就越强。
当电负性差大于1.6时,电子完全被一个原子占有,即形成离子键。
同样,当电负性差在0.4和1.6之间时形成极性共价键,当电负性差在0.4以下时形成非极性共价键。
在周期表中,电负性在一列中从上到下递减,在一列中从右到左递减。
NH4Cl中化学键的类型
氯化铵是一种化合物,它的不同原子之间有三种键。如前所述,离子键存在于铵离子和氯离子之间。
此外,与氮原子相连的三个氢原子中的每一个都与氮原子平等地共享电子。这是因为电负性差非常小。而且,这两个原子都是非金属。因此,氯化铵分子中存在三个共价键。
另外,最后一个氢原子通过配位共价键连接到氮原子上。这也被称为给键,当参与成键的两个电子都是由同一个原子给出时,就形成了给键。
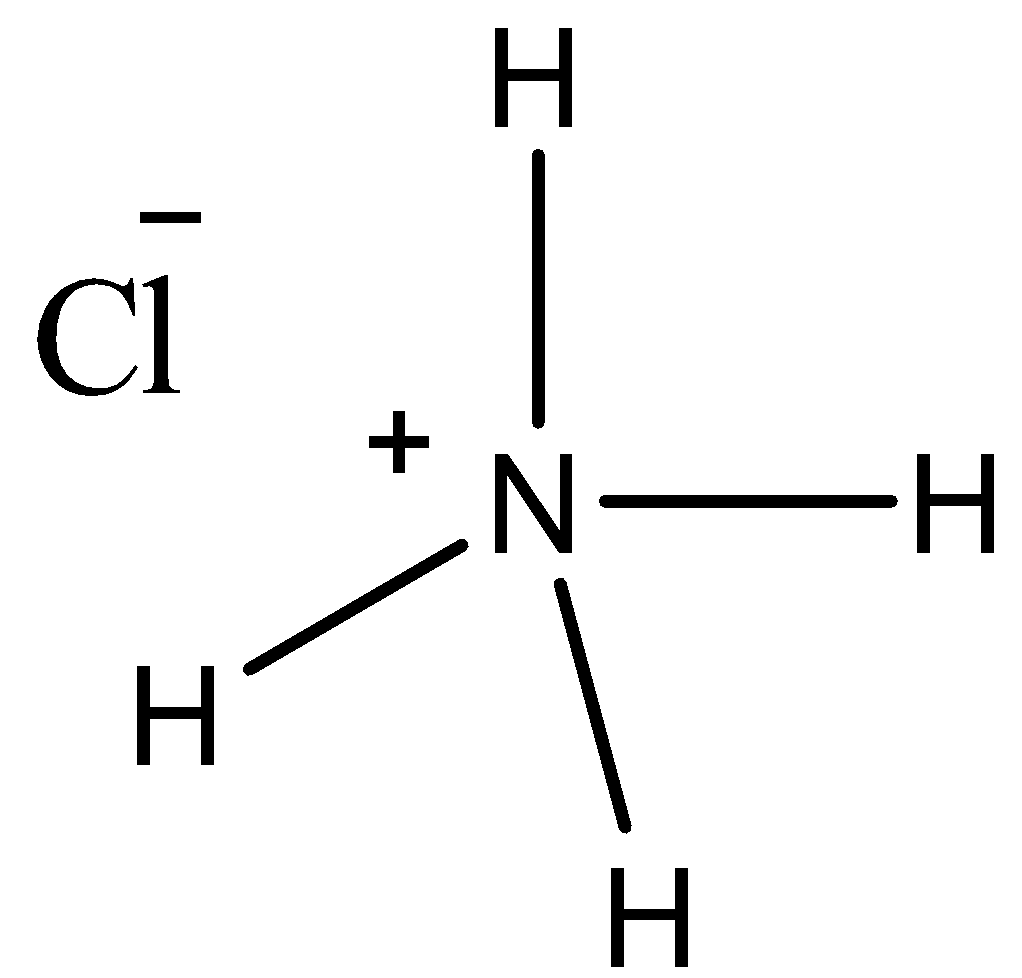
氯化铵分子的成键过程如下图所示:

在上图中:
•1是共价键。
•2是一个坐标共价键。
•3是离子键。
同样,我们也可以画出氯化铵的Lewis结构:

从上面的结构中可以看出,最初有7个电子的氯原子现在已经变得稳定,因为它的价电子层中有8个电子。
类似地,氮原子从一个氢原子那里得到了一个额外的电子,在得到一个正电荷后,它就稳定了。
常见问题
问:氯化铵加热后会发生什么?
答:经过加热,氯化铵分子分解成氨和氯化氢气体。
问:氯化铵对人体有害吗?
答:是的。众所周知,当人接触氯化铵时,会引起类似哮喘的症状。在长期接触下,它还会损害肾脏。不仅是人类,它对水生生物也有不利影响。
问:氯化铵摸起来安全吗?
答:NH4Cl本质上是酸性的。虽然,它可能不会造成像盐酸这样的强酸那样严重的损害,但接触它仍然是危险的。暴露在眼睛里会引起刺激。
问:为什么漂白剂和氯化铵混合是危险的?
答:氯化铵和漂白剂的混合物会释放出氯胺气体。它在本质上是有毒的,暴露时对眼睛、鼻子、喉咙等造成刺激。
问:你在房子里的什么地方能找到氯化铵?
答:氯化铵是许多日常产品的一部分,如洗发水、染发剂、洗面奶、洗碗液等。
NH4Cl的性质
氯化铵的几个重要性质如下:
•NH4氯的分子质量为53.49克/摩尔
•它以吸湿白色固体的形式出现。
•它是一种无味的结晶盐。
•NH的密度4氯是1.519克/厘米3.
•呈微酸性,pH值在4.5到6之间。
•NH的熔点和沸点4Cl分别为338°C和520°C。
NH4Cl的用途
氯化铵最常见的用途是作为肥料。
•它被用作止咳药中的祛痰剂。
•用于实验室冷却浴中保持低温。
•它也被用作牛饲料的补充。
相关的话题
结论
氯化铵是一种离子化合物,它是在氨(多原子离子)和氯(金属)之间形成的键。
氯化铵分子也由三个共价键组成,存在于氮和三个氢原子之间,以及氮和氢原子之间的一个坐标共价键。
在离子化合物中,两个结合原子之间的电负性差大于1.6。然而,在极性共价键的情况下,这个差异在0.4到1.6之间,而对于非极性共价键,它低于0.4。




