四氟化硫是一种化学式为SF4的化合物。这种化合物以无色气体的形式存在。它也被认为是最好的有机氟化剂之一。很多人可能会怀疑SF4是极性的还是非极性的。在本文中,我们将找出这个问题的答案,并将研究它的性质和应用。
那么,SF4是极性的还是非极性的?SF4(四氟化硫)本质上是极性的,因为硫原子上有一个孤对,因此分子的形状变得不对称;跷跷板。氟的电负性比硫强,分子整体电荷分布不均匀,形成极性分子,偶极矩为0.632 D。
四氟化硫是一种化合物,其IUPAC系统名称为氟化硫(IV)。
这种化合物富含氟,因此被认为是最好的氟化剂之一。
SF4的分子质量为108.07 g/mol。考虑如下
SF4的Mol质量= 1 * (32)S的Mol质量+ 4 * (18.9)F的Mol质量= 108.07 g/ Mol。
如果我们讨论四氟化硫的化学组成,它由1个硫原子和4个氟原子组成。
硫原子有6个价电子,其中4个电子参与了与4个氟原子形成的sigma键,2个电子形成孤对。
氟原子有7个价电子,还需要1个电子来完成它的八隅电子,它从硫原子中分享了1个电子,在硫原子上留下了1个孤对。
结果,孤对和键对之间发生电子排斥,形成的分子的几何形状是跷跷板。
由于分子形状不对称,SF4分子间电荷分布不均匀。
此外,氟和硫的电负性不同,硫的电负性为2.58,氟的电负性为3.98。
氟的电负性更强,对成键电子对的吸引作用更大,获得部分负电荷,其他原子获得部分正电荷。
极性分子和非极性分子
结合分子的力有不同形式。这些力包括离子键、共价键、金属键和氢键。
共价键的分子可以是极性的也可以是非极性的。让我们讨论一下极性分子和非极性分子之间有什么不同。
极性分子这些分子的原子间电荷分布不均匀。这些分子的偶极矩总是等于非零。
这些分子中原子的电负性是不相等的,因为这些原子对成键电子对有不相等的影响。
如果两个原子的电负性不同,它们形成的共价键就趋向于极性。
通常可以看到极性分子的几何形状是不对称的。
这些分子的例子有H2O, SO2。你可以查看原因SO2极性.
非极性分子如原子间电荷分布均匀的分子称为非极性分子。
形成非极性共价键的两个原子的电负性是相等的,因为两个原子都有相等份额的成键电子对。
一般认为非极性分子的几何结构是对称的。
这类分子的例子有XeF2、O2等。你可以查看原因XeF2无极性.
为什么SF4是极性的?
如上所述,分子的几何形状是表明其极性的重要因素。
如果我们检查VSEPR图,硫原子由1个孤对组成,因此SF4的形状变得不对称,即;跷跷板。
氟的电负性比硫强。氟原子更倾向于吸引成键的电子对并获得部分负电荷而硫原子则获得部分正电荷。
这样,SF4分子原子上的电荷分布就变得不规则了。
氟原子一侧变成负极,中心原子(硫)变成正极。
SF4的偶极矩为0.632 D。
点检查一个化合物的极性
电负性原子的电负性是指原子吸引成键电子对的强度。一个原子的电负性越大,它就越能吸引电子到它的一边。
如果组成一个分子的两个原子的电负性不同,这个分子就会形成极性分子,因为它的原子所占的电荷份额不相等。
因此,分子的极性与它们的电负性之差成正比,反之亦然。
但在对称几何的情况下,具有不等电负性的分子也可以是非极性的,因为在这种情况下,偶极子由于对称形状而相互抵消。
几何形状分子的几何形状也是检验化合物是否极性的重要参数。
极性分子通常具有不对称的几何形状,因为它们具有不平等的电荷分布。
而非极性分子具有对称几何。
即使一个分子由不同电负性的原子组成,它也有可能是非极性的,因为在这种情况下,由于对称的形状,这种键的偶极子会相互抵消。
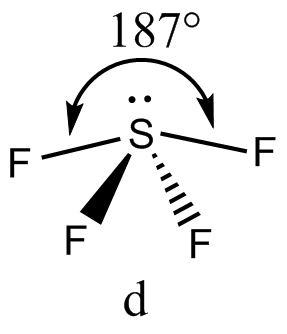
下图是SF4分子的几何结构形状。
偶极矩分子的偶极矩是其极性的量度。分子的极性与其偶极矩成正比。
它被计算为原子上的电荷和正负电荷中心之间的距离的乘积。
D = q * r
SF4的性质
- 四氟化硫在室温下以气态存在。
- 它的外观无色,被认为是剧毒。
- 在−78℃的温度下,其密度为1.95 g/cm3。
- 该物质的熔点为- 121.0℃,沸点为- 38℃。
- 在22℃的温度下,该物质的大气压为10.5 atm。
- SF4的分子形状为“跷跷板”。
- SF4的偶极矩约为0.632 D。
SF4的用途
- 在有机合成中,四氟化硫被认为是制备有机氟化合物的试剂。
- 广泛用于羰基和羟基的氟化。
- 也应用于生物领域中制造高端液晶材料的医药。
- 它也被用于制造杀虫剂。
结论
四氟化硫由1个硫原子和4个氟原子通过sigma键连接。硫原子由1个孤对组成。
结果,由于孤对和键对的电子斥力,分子的形状变得不对称。跷跷板。
其次,氟原子和硫原子的电负性有很大的差异,氟原子获得部分负电荷,硫原子获得部分正电荷。
由于这些因素,四氟化硫是极性分子。
所以朋友们,如果你有任何疑问,请通过评论提出你的疑问。我会很快联系你的。




