三氧化二硫也被称为nisso sulfan,用化学式SO表示3..它是无色至白色的结晶固体,与水发生剧烈反应。它也以气态和液态形式出现,并在空气中产生烟雾,形成有毒蒸汽。
它对金属有腐蚀性,对人的眼睛和皮肤有刺激性。它以单体形式存在,也以聚合物形式存在。在经济上,它也被认为是最重要的硫氧化物。
它被用于油漆的制造、电气设备、水处理、建筑和建筑材料、空气排放控制等。
你好大家! !在本文中,我们将回答您有关三氧化硫的问题。
所以请继续阅读....
是如此的3.共价还是离子?三氧化硫是一种共价化合物。以三氧化硫为例,键是在两种非金属之间形成的,即硫和氧,电子被参与的原子共享。因此,分子中形成的键本质上是共价的。
然而,硫的电负性是2.58,而氧的电负性是3.44,这是因为两个原子之间的电子不是平均分配的。这种电负性差异导致极性共价键的形成,尽管分子本身是非极性的。
我们将在接下来的章节中研究原因和方法。
SO3含有什么类型的键?
在回答这个问题之前,我们必须先了解原子究竟为什么会成键。
实际上,每个原子都有趋于稳定的趋势。由于原子的稳定性取决于其价壳层中电子的数量,因此每个原子都倾向于完成它的八隅体。这就是化学键形成的原因。
在化学键中,原子根据需要获得、失去或共享电子。
原子吸引电子的能力,在形成键的过程中,被称为它的电负性。
参与成键的两个原子的电负性的不同决定了所形成的键的性质。
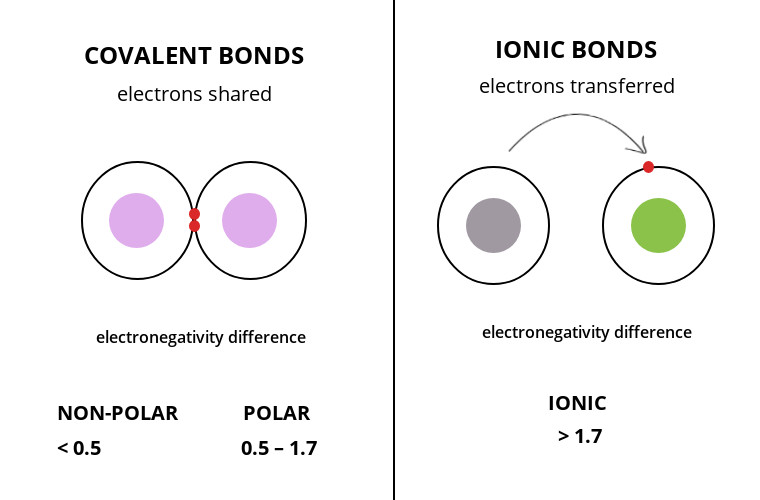
通常,电负性差在1.6以上的原子形成离子键,电负性差在1.6以下的原子形成共价键。
然而,共价键进一步分为极性共价键和非极性共价键。

如果成键原子的电负性差在0.4 ~ 1.6之间,则成键为极性共价键,而电负性差在0.4以下,则成键为非极性共价键。
在极性共价键中,共用的电子对轻微地移向电负性更强的原子。
因此,部分负电荷在电负性强的原子上形成,而部分正电荷在电负性弱的原子上形成。这些电荷用符号δ+表示部分正电荷,用符号δ-表示部分负电荷。
另一方面,在非极性共价键中,电子在两个结合的原子之间或多或少地平分。
以三氧化硫为例,硫的电负性为2.58,而氧的电负性为3.44。因此,电负性差约为0.86。由于这个差值在0.4和1.6之间,所以在SO中形成了键3.分子是极性共价键。
然而,三氧化硫分子上的净电荷由于其几何形状为零,因此分子本身是非极性的。
继续阅读,了解更多…
为什么SO3是共价分子?
通常,当两种非金属之间形成一个键时,它就是共价键。以三氧化硫为例,硫和氧都是非金属。因此,这两个原子之间形成的键是共价键。
此外,硫和氧都属于元素周期表的第16族,最外层都有6个价电子。因此,这两个原子都需要两个电子来完成它们的八隅体。
此外,硫和氧的电负性差在1.6以下。
正如我们在前一节中已经研究过的,当电负性差高于1.6时,离子键形成,而当电负性差低于1.6时,共价键形成。
因此,它进一步表明,在SO中,氧原子和硫原子之间形成了键3.分子是共价的。
共价键和离子键
到目前为止,我们已经研究了很多共价键和离子键形成的原因和方式。在本节中,我们将进一步研究这两种化学键之间的区别。
原子形成键来稳定自身,许多因素决定了形成键的性质和特征。让我们来学习如何:
•从名称上可以清楚地看出,离子键涉及离子之间的键,而共价键涉及不同的原子。
•离子键形成于两种金属之间,或金属和非金属之间,或金属和多原子离子之间。另一方面,两种非金属之间形成共价键。
•当一个原子将其电子或电子捐赠给另一个原子时,离子化合物就形成了,而当参与原子之间共享电子时,就形成了共价键。
•当参与成键的原子的电负性之差大于1.6时形成离子键,而当电负性之差小于1.6时形成共价键。
•离子键只有一种类型,而共价键可以进一步分为极性和非极性共价键,根据参与原子的电负性的不同。
当参与原子的电负性差在0.4和1.6之间时,极性共价键就形成了。但是,如果电负性差小于0.4,则形成非极性共价键。
•当离子化合物溶解在水溶液中,通常会形成一个正离子(阳离子)和一个负离子(阴离子)。另一方面,共价化合物通常不溶于水。
•一般来说,离子化合物是热电的良导体,而共价化合物是热电的坏导体。
•离子化合物的熔点和沸点通常比共价化合物高。
•离子化合物在室温下主要以固体形式存在,而共价化合物则以液体或气体形式存在。
•离子化合物的一些例子是NaCl, NaCN, NH4Cl等,而一些共价化合物的例子是SO3.H2啊,等等。
为什么SO3不是离子型的?
如前一节所讨论的,当参与键形成的两个原子的电负性之差大于1.6时,离子化合物就形成了。
此外,当一个金属原子与另一个金属原子、非金属原子或多原子离子结合时,离子键就形成了。
在三氧化硫的情况下,参与的原子,即氧和硫都是非金属,这表明这两个原子之间形成的键不可能是离子。
此外,这两个原子之间的电负性差小于1.6。因此,三氧化硫不是离子化合物。
相关的话题
SO3是极性还是非极性?
到目前为止,我们已经讨论了硫原子和氧原子之间形成的键,在三氧化硫分子中是共价键。
我们还了解到,这个键本质上是极性的,因为硫原子和氧原子的电负性差在0.4和1.6之间。因此,这种键被称为极性共价键。
然而,令你惊讶的是,SO3.分子本身是非极性的。
想知道吗?让我解释一下
实际上,根据VSEPR理论,SO的分子几何结构3.分子是三角形平面。因此,SO3.分子结构如下:

从上图中可以看出,硫原子和氧原子之间的三个双键(S=O)彼此处于120°角。
因此,由于两个原子之间的电负性差异,S=O键中产生的极性相互抵消。
因此,三氧化硫分子的整体极性变为零,而SO3.分子成为非极性在自然界中。
结论
三氧化硫分子是共价因为参与的原子,即硫和氧都是非金属。
•硫和氧原子的电负性之差在0.4和1.6之间。因此,化学键是极性共价键。
•SO3.分子是非极性的,因为三氧化硫的几何形状是三角平面,三个S = O键彼此呈120°角。因此,化学键的极性相互抵消。




