四氯化硒是由一个硒原子和四个氯原子组成的无机化合物。硒属于第16类,氯属于第17类。
它是一种黄白色的挥发性固体,溶于水。
在这篇文章中,我们将了解所需的基本概念,以预测刘易斯结构,几何,杂化和极性的给定物质。
路易斯结构
刘易斯结构是化合物中原子排列的二维表示形式。它显示了单个原子周围电子的排列。
根据Lewis,只有价电子参与键的形成,因此只有价电子用Lewis符号表示。
一个化合物可以有多个可能的路易斯结构。在这种情况下,我们寻找满足八隅体规则和形式电荷的结构。
八隅体规则
所有主族元素的原子都倾向于有8个价电子(周期1元素除外)以获得稳定。这种对8个电子的偏好被称为八隅体规则。
18族元素被认为是最稳定的,有8个价电子(He除外)。因此,其他基团的元素更倾向于有8个价电子,具有像惰性气体一样的稳定性。
八隅体规则对于稳定的Lewis结构很重要,但许多化合物永远不能遵循八隅体规则,而是稳定的。八隅体规则不能解释-的稳定性
•次价化合物——中心原子缺乏电子,它的八隅体永远不能完成。例如AlCl3.等。
•高价化合物-中心原子由于八隅体的膨胀而富电子,中心原子上有8个以上的价电子。例如,SF6,等。
•奇数电子种-一些分子有奇数电子,永远不能达到八隅体,因为它们不能有偶数个电子。例如,NO,等等。
形式电荷
这是一个理论概念。它将孤立的中性原子上的电子与化合物中原子上的电子进行比较。形式电荷的公式是
形式电荷=(孤立原子中价壳电子总数)-(非成键电子数)- 0.5*(成键电子数)
负形式电荷在电负性原子上比在电正性原子上更稳定,反之亦然。
绘制给定化合物路易斯结构的步骤
1.首先,数一数每个原子的价层电子数。在画路易斯结构之前,我们需要知道所有组成原子的价壳电子的数量和它们的总和。
| 原子 | 原子序数 | 集团 数量 |
价 电子 根据组别 数量 |
电子 配置 (。) |
e。c。价层 | 价 电子来自e.c。 |
| 一个Se | 34 | 16 | 6 | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p4 | n = 4 | 6 |
| 四氯 | 17 | 17 | 7 | 1s2 2s2 2p6 3s2 3p5 | n = 3 | 7 |
| 价层电子总数= 6 + (7*2)= 20 | ||||||
2.绘制元素的路易斯点结构。
我们通过排列元素化学符号周围的价壳电子来画出元素的路易斯结构。
硒和氯的化学符号分别是Se和Cl。Se和Cl的路易斯点结构如下


3.为化合物选择一个合适的中心原子。
我们必须仔细选择中心原子。它一定是电负性最小的原子从组成原子中。在氯和硒之外,氯的电负性更强,不能成为中心原子
如果中心原子的电负性比旁边的原子大,中心原子就会保持电子密度偏向它自己。
因此,硒是这种化合物的中心原子。
4.画一个骨架图。
在这一步中,我们必须适当地安排侧原子和中心原子。

5.将价电子排列在元素符号周围。
总价层电子(在步骤1中计算)是根据预测的键的形成。

6.在相邻原子之间形成键,并尝试完成所有的八隅体
Se在孤立态有6个价电子。它和每个氯共用一个电子。由于d轨道的可用性,它可以扩展八隅体。因此,该化合物中的硒不满足八隅体规则。
每个氯原子在价层有7个电子处于自由态,它与硒共用一个电子,形成满电子构型。

7.计算所有原子的形式电荷。
这个化合物的净电荷是零。
| 原子 | 的数量 价电子层的电子 根据元素周期表 |
的数量 电子 孤对 |
(数量的 电子 参与 结合)* 0.5 |
形式电荷 在原子 |
|---|---|---|---|---|
| Se | 6 | 2 | 8 * 0.5 = 4 | 6-2-4 = 0 |
| Cl1 | 7 | 6 | 2 * 0.5 = 1 | 7-6-1 = 0 |
| 这有点难度 | 7 | 6 | 2 * 0.5 = 1 | 7-6-1 = 0 |
| Cl3 | 7 | 6 | 2 * 0.5 = 1 | 7-6-1 = 0 |
| Cl4 | 7 | 6 | 2 * 0.5 = 1 | 7-6-1 = 0 |
因此,在步骤6中绘制的结构是SeCl4的最佳Lewis结构。
SeCl4几何
分子几何是指分子中原子在空间中的三维排列。VSEPR理论有助于确定给定化合物的形状和几何形状。
VSEPR理论是价壳电子对排斥理论的缩写。
该理论基于这样的原理:分子中每个原子的价壳电子以电子间斥力最小的方式排列,并且排列变得稳定。这种稳定的排列被称为几何。
几何和形状常常互相混淆。几何是指电子的键对排列,形状是指电子的键对和孤对排列。
如何用VSEPR预测sec4几何
1.首先,我们必须计算中心原子的价层电子数,并让它们等于A(任意变量)。
在SeCl的情况下4时,中心原子为Se。硒有6个价电子。(如绘制lewis结构step1所示)
= 6
2.计算侧原子的数量,让它等于B(任意变量)。在SeCl4,有四个边原子,B=4
3.如果该化合物带电荷,带正电的化合物从B中减去电荷,带负电的化合物在B中加上电荷。对于中性化合物可以避免这一步。
在SeCl4,没有电荷,只有B=4。
4.将侧原子和电荷的贡献与中心原子的贡献相加,即A+B
对于SeCl4,A + B = 10
5.将A+B除以2,得到影响形状的电子对总数。
对于SeCl4,有5个电子对。
6.把总电子对分为成键电子对和非成键电子对。成键电子对等于侧原子的数目。
对于SeCl4,有四个侧原子。因此,有四个成键电子对和一个非成键电子对。
使用这些信息,可以很容易地找到SeCl的几何和形状4从下面的表格。
电子几何是三角锥体,形状是跷跷板。孤对化合物的几何和形状是不同的。


SeCl4杂交
杂化是解释化学键形成的基本概念之一。
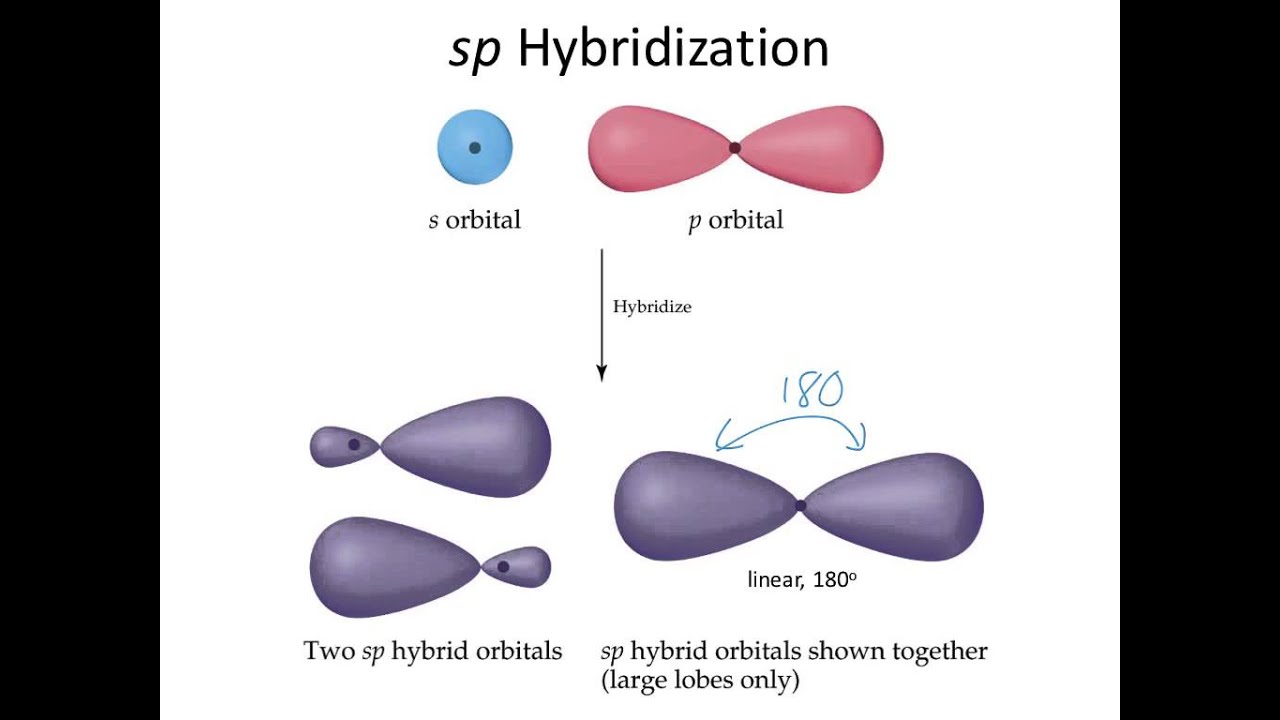
杂化是将两个或多个具有相对能量、大小和形状的原子轨道混合,形成具有相同能量、形状和大小的轨道。
杂化轨道形成键,重叠程度优于未杂化轨道。
例如,一个4s轨道和一个4p轨道可以形成两个sp杂化轨道,但4s轨道和8d轨道不能。
在SeCl4, Se是中心原子。我们只关注中心原子的杂化。
在基态,Se有2个未配对电子。它只能形成两个键。电子从4p跃迁到4d,有4个价电子未成对。

空间数法
空间数是指中心原子上电子对的总数。
对于SeCl4,电子对=5(使用VSEPR预测几何时显示)
空间数= (sigma键+中心原子孤对)的数目
SeCl的空间数4= (4 + 1) = 5
杂化就是sp3.D从桌子上。

SeCl4极性
如果一个化合物的净偶极矩不为零,它就是极性的;如果一个化合物的净偶极矩为零,它就是非极性的。
净偶极矩的准确值可以通过将分子中所有键的偶极矩矢量相加得到。
键的偶极矩可以用公式计算
偶极矩=电荷*电荷之间的分离距离
我们不需要计算偶极矩的确切值来确定极性,但可以对化合物进行定性评估。
化合物的偶极矩取决于
•偶极矩,这反过来取决于原子形成键的电负性之间的差异。
•化合物的几何形状
在SeCl4,只形成了一种键:“Se-Cl”。
Se和Cl的电负性分别为2.55和3.16。差值是0.61。因此,化学键是极性的。
极性键并不能保证分子是极性的。我们还考虑了化合物的几何和对称性。它的形状是一个跷跷板,键向量不会互相抵消。因此,化合物是极性的。
相关的话题
结论
四氯化硒是一种共价化合物。
上面所画的Lewis结构是最合适的。硒膨胀八隅体,是一种超价化合物。
化合物的几何形状是三角金字塔,形状是一个跷跷板。中心原子的杂化是sp3.d。
它是极性化合物。
阅读的快乐!




